Welke drie soorten ontleedbare stoffen (verbindingen) zijn er?
Leerdoelen
•Je kunt uitleggen welke soorten ontleedbare stoffen er zijn.
•Je kunt uitleggen hoe positieve en negatieve ionen ontstaan.
•Je kunt de lading van ionen geven.
•Je kunt een verhoudingsformule voor zouten maken.
Wat zijn ontleedbare stoffen?
Er zijn stoffen die je wel kunt ontleden en stoffen die je niet kunt ontleden. Gewone elementen, zoals losse atomen, kun je niet ontleden. Een atoom is een atoom; daar kun je geen half atoom van maken. Maar als atomen aan elkaar vastzitten met een verbinding, kun je die verbindingen wel ontleden. Stoffen die bestaan uit meerdere elementen en die je kunt ontbinden, noemen we een ontleedbare stof.
De drie soorten verbindingen
•Moleculaire verbindingen: dit is als een niet-metaal aan een ander niet-metaal vastzit. Denk bijvoorbeeld aan water (H2O), waarbij waterstof (H) en zuurstof (O) beide niet-metalen zijn.
•Ionaire verbindingen (zouten): een zout mag ook een ionaire verbinding genoemd worden. Dit type verbinding ontstaat als een niet-metaal (vaak negatief geladen) en een metaal (meestal positief geladen) aan elkaar verbonden zijn. Een bekend voorbeeld is keukenzout (NaCl).
•Metalen: dit zijn verbindingen waarbij twee (of meer) metalen aan elkaar vastzitten, zoals in een legering of een puur metaalrooster.
Ionen: geladen atomen
Ionen zijn elektrisch geladen atomen. Een neutraal atoom heeft evenveel positief geladen protonen in de kern als negatief geladen elektronen die eromheen bewegen. Als dit evenwicht verstoord raakt, wordt het atoom een ion.
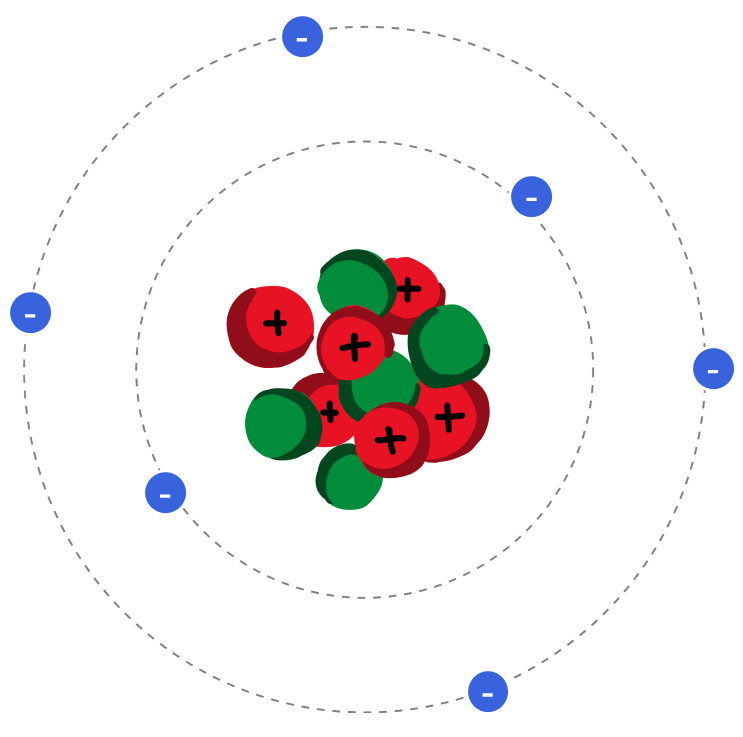
Hoe ontstaan positieve ionen?
Een atoom wordt positief geladen als het meer protonen (plusjes) dan elektronen (minnetjes) heeft. Dit gebeurt wanneer een atoom elektronen verliest. Stel, je hebt een neutraal atoom met zes plusjes en zes minnetjes. Als één van die minnetjes (elektronen) weggaat, heb je nog maar vijf minnetjes, en nog steeds zes plusjes. Er is nu één plusje meer dan minnetjes, dus is het positief geladen atoom. Dit noemen we een positief ion.
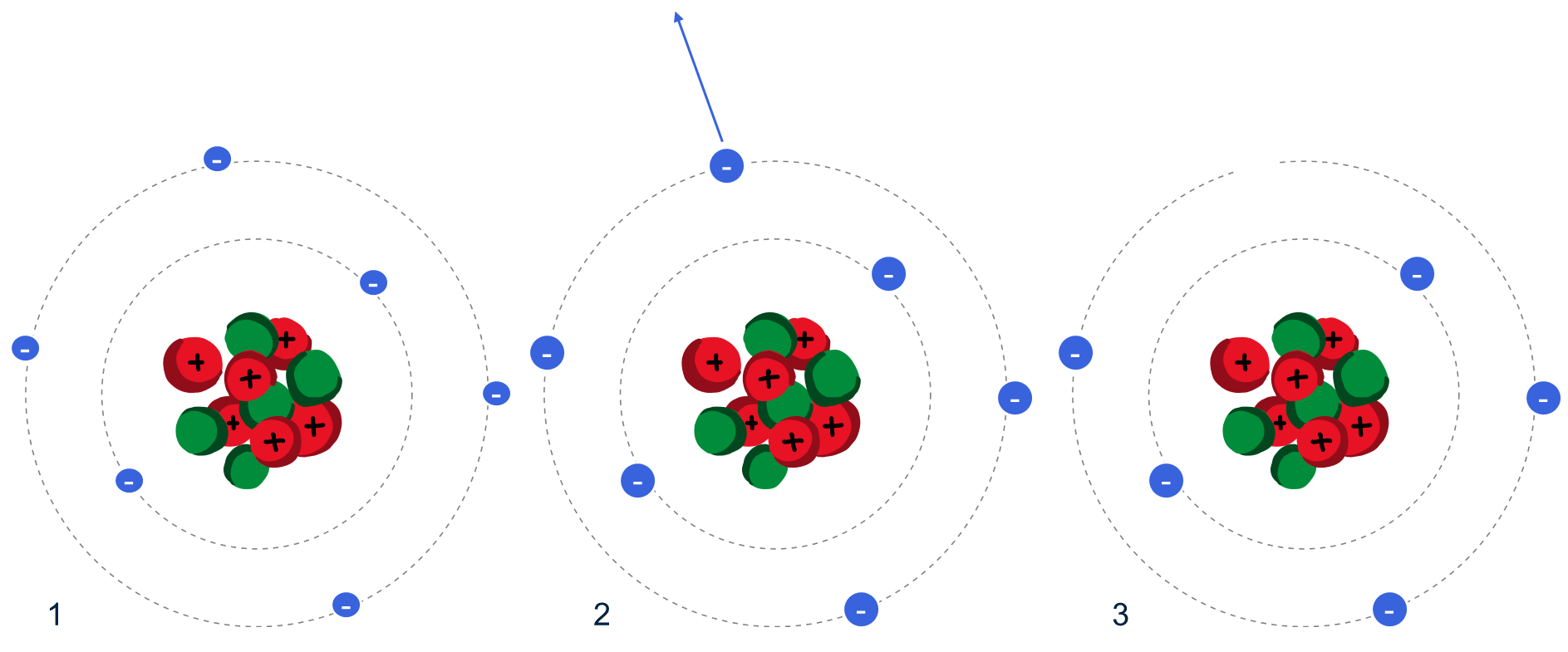
Hoe ontstaan negatieve ionen?
Een atoom wordt negatief geladen als het meer elektronen (minnetjes) dan protonen (plusjes) heeft. Dit gebeurt wanneer een atoom extra elektronen opneemt. Stel dat er bij het neutraal atoom een extra elektron bijkomt, dan heb je zeven minnetjes en zes plusjes. Er is nu één minnetje meer dan plusjes, dus is het negatief geladen atoom. Dit noemen we een negatief ion.
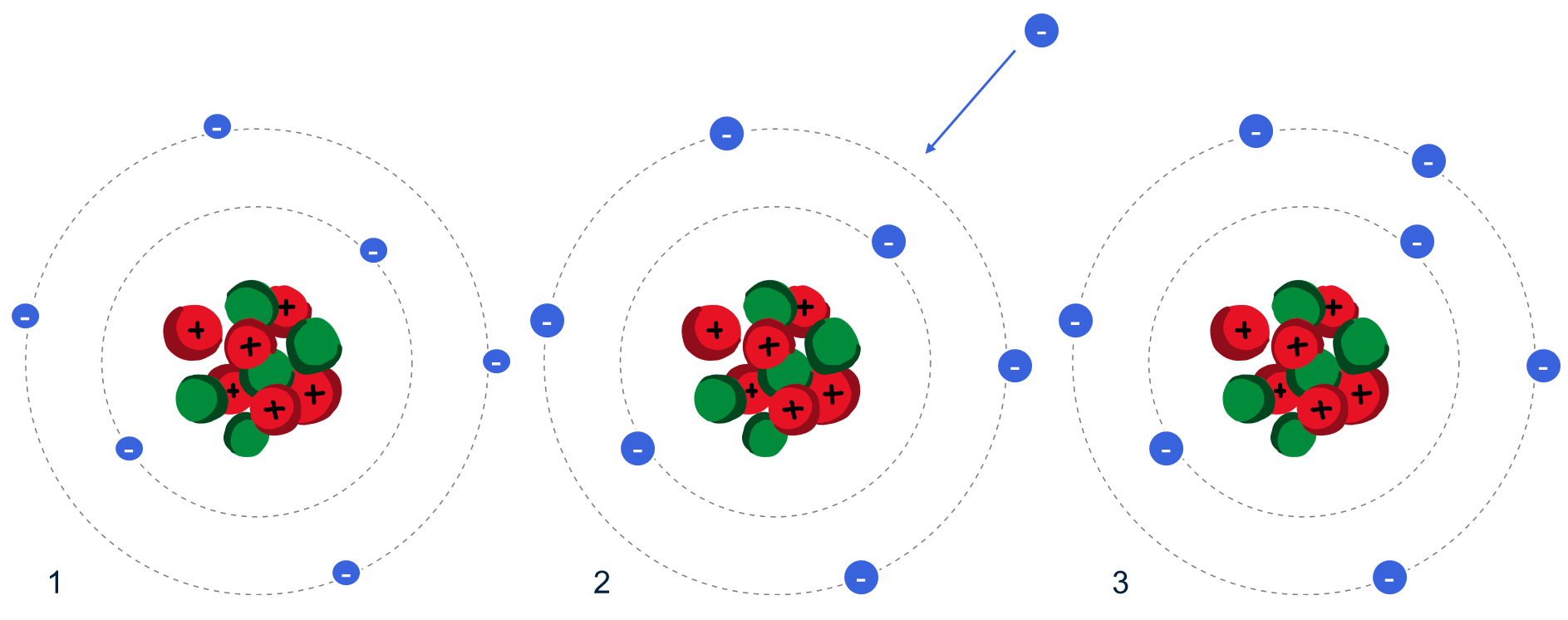
De lading van ionen bepalen
Element | Ion | Element | Ion |
zilver | Ag+ | broom | Br- |
kalium | K+ | chloor | Cl- |
natrium | Na+ | fluor | F- |
barium | Ba2+ | jood | I- |
calcium | Ca2+ | zuurstof | O2- |
koper | Cu2+ | zwavel | S2- |
magnesium | Mg2+ | ||
lood | Pb2+ | ||
tin | Sn2+ | ||
zink | Zn2+ | ||
aluminium | Al3+ | ||
ijzer(II) | Fe2+ | ||
ijzer(III) | Fe3+ |
Je kunt de lading van de meest voorkomende ionen uit je hoofd leren. Je kunt ook een trucje gebruiken met de Binas en het periodiek systeem. Het is handig, maar het werkt niet voor alles, dus sommige moet je wel uit de tabel leren.
Kijk naar de groepen (kolommen) in het periodiek systeem:
Vanaf de linkerkant van het periodiek systeem:
Groep 1: deze elementen vormen ionen met een lading van +1.
Groep 2: deze elementen vormen ionen met een lading van +2.
Groep 3: deze elementen vormen ionen met een lading van +3.
Vanaf de rechterkant van het periodiek systeem:
Groep 18 (de edelgassen): deze hebben geen lading (0), ze reageren bijna niet.
Groep 17: deze elementen vormen ionen met een lading van -1.
Groep 16: deze elementen vormen ionen met een lading van -2.
Onthoud dat dit een trucje is en niet voor alle elementen geldt.
Verhoudingsformule van zouten maken
Een belangrijk kenmerk van een zout is dat het altijd neutraal is. Dat betekent dat de totale positieve lading en de totale negatieve lading in het zout precies even groot zijn. Als je een zout formuleert, moet je ervoor zorgen dat er evenveel plusjes als minnetjes zijn.
Stappenplan voor een verhoudingsformule:
Laten we als voorbeeld het zout aluminiumbromide nemen.
Stap 1: Schrijf de symbolen van de ionen en hun lading op. Schrijf altijd het positieve ion eerst. Je zoekt de symbolen op. Gebruik de Binas of de geleerde tabel.
•Aluminium-ion: Al³⁺
•Bromide-ion: Br⁻
Stap 2: Zorg ervoor dat de totale lading neutraal is (evenveel plus als min). Je hebt nu 3 plusjes (van Al³⁺) en 1 minnetje (van Br⁻). Om dit neutraal te maken, heb je meer bromide-ionen nodig.
•Als je één Al³⁺ hebt, heb je drie Br⁻-ionen nodig om de lading neutraal te maken (3 x -1 = -3).
•De totale positieve lading is dan 3+ en de totale negatieve lading is 3-. Samen is dit 0, dus neutraal.
Stap 3: Schrijf de verhoudingsformule netjes op. Zodra je weet hoeveel ionen van elke soort je nodig hebt, schrijf je de formule op zonder de ladingen. Het aantal van elk ion zet je rechtsonder het symbool als een klein getal, de index. Als je maar één van een ion hebt, schrijf je het getal 1 niet op.
•We hebben 1 aluminium-ion (Al).
•We hebben 3 bromide-ionen (Br).
De verhoudingsformule wordt dan AlBr₃.













