Waarom kan je ervan uitgaan dat je sandwich ham-kaas 150 gram weegt als de afzonderlijke onderdelen 100, 25 en 25 gram wegen?
Leerdoelen
•Je kunt de wet van behoud van massa uitleggen.
•Je kunt de massa van een stof berekenen met behulp van een verhoudingstabel.
Wat is massabehoud?
Massabehoud betekent dat de totale massa vóór een chemische reactie precies evenveel is als de totale massa ná die reactie. Massa kan namelijk niet zomaar verdwijnen; het gaat altijd ergens naartoe.
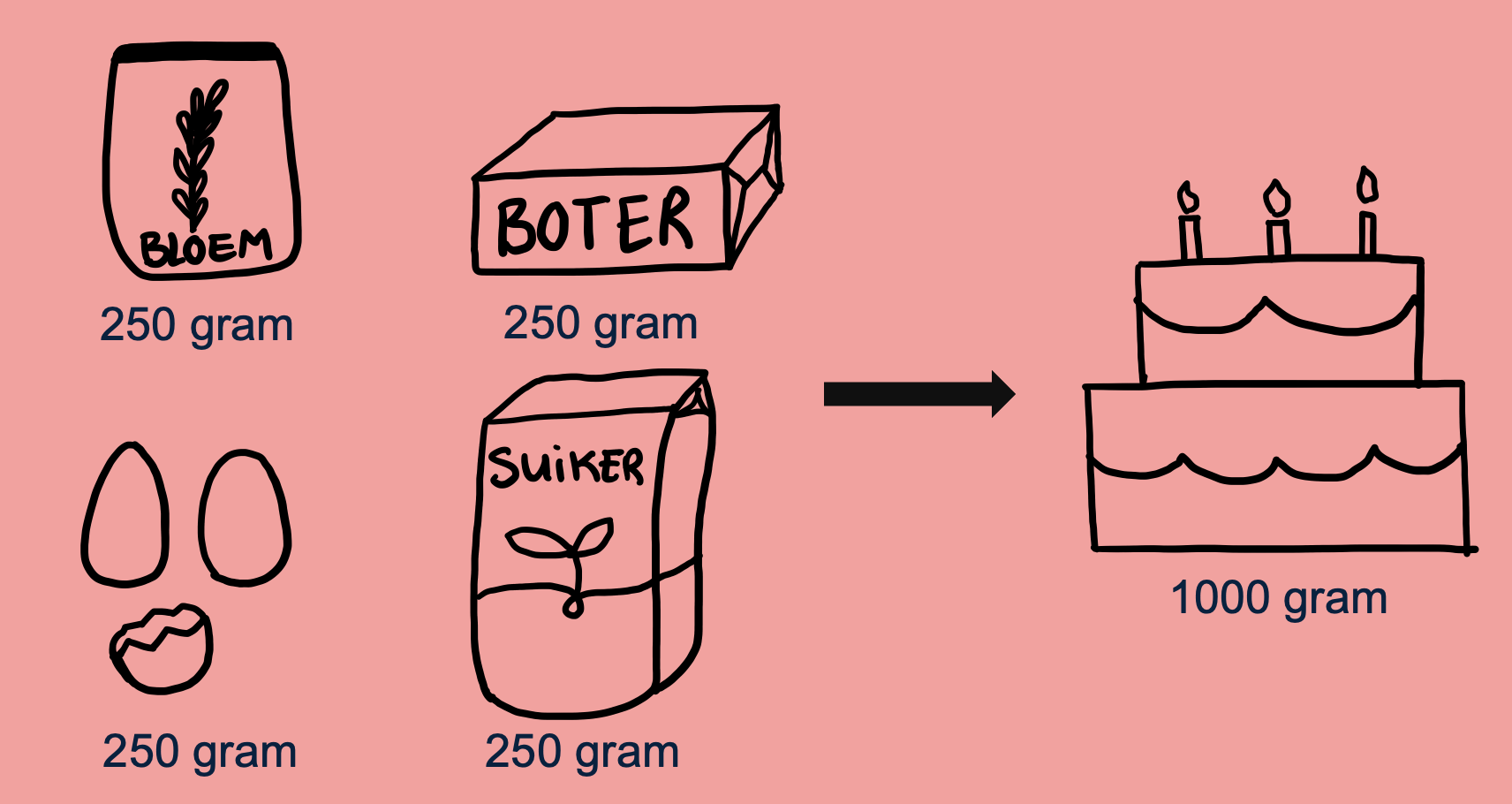
Stel je voor dat je een cake bakt. Als je bijvoorbeeld 250 gram bloem, 250 gram suiker, 250 gram boter en 250 gram eieren gebruikt, heb je in totaal 1000 gram (oftewel 1 kilogram) aan ingrediënten. Na het mengen en bakken in de oven krijg je precies 1 kilogram cake. De massa is niet verdwenen, de ingrediënten zijn alleen veranderd in een heerlijke cake. Dit is een simpel voorbeeld van de wet van behoud van massa.
Rekenen met verhoudingen
In de scheikunde werken we met ingewikkelde stoffen en precieze berekeningen. Om te weten hoeveel stof je nodig hebt, gebruiken we verhoudingen. Een verhouding vertelt je de exacte hoeveelheid van elke stof die deelneemt aan een reactie.
Voorbeeld
Bij de ontleding van 7 gram ijzeroxide (Fe₂O₃) ontstaat 5 gram ijzer (Fe) en 2 gram zuurstof (O₂). Dit betekent dat je om 5 gram ijzer te maken 7 gram ijzeroxide nodig hebt.
Deze verhouding kunnen we ook laten zien in een reactievergelijking: Fe₂O₃ → Fe + O₂ De verhouding in grammen is dan: 7 gram (Fe₂O₃) → 5 gram (Fe) + 2 gram (O₂)
Met deze verhoudingen kun je rekenen, want je hebt niet altijd precies 7 gram ijzeroxide. Soms wil je bijvoorbeeld weten hoeveel ijzeroxide je nodig hebt om 28 gram ijzer te maken. Hiervoor gebruiken we een verhoudingstabel.
De verhoudingstabel stap voor stap
Met een verhoudingstabel kun je de massa van stoffen berekenen als je de verhouding en één bekende massa hebt. Dit doe je door gebruik te maken van de volgende stappen:
Stap 1: Tabel maken
Maak een tabel met vier kolommen. Geef ze de volgende titels:
•Stofnaam
•Verhouding (gram)
•Tussenstap (naar 1 gram)
•Gevraagde massa (gram)
Stofnaam | Verhouding | Tussenstap | Gevraagde massa (gram) |
|---|---|---|---|
Stap 2: Stofnamen invullen
Vul in de kolom 'Stofnaam' de namen van de stoffen in die bij de reactie betrokken zijn. In ons voorbeeld zijn dat ijzeroxide, ijzer en zuurstof:
Stofnaam | Verhouding | Tussenstap | Gevraagde massa (gram) |
|---|---|---|---|
ijzeroxide | |||
ijzer | |||
zuurstof |
Stap 3: Verhoudingen invullen
Vul de bekende verhoudingen in de kolom 'Verhouding (gram)' in. We weten dat 7 gram ijzeroxide zorgt voor 5 gram ijzer en 2 gram zuurstof:
Stofnaam | Verhouding | Tussenstap | Gevraagde massa (gram) |
|---|---|---|---|
ijzeroxide | 7 | ||
ijzer | 5 | ||
zuurstof | 2 |
Stap 4: Gevraagde massa invullen
Vul de bekende massa in de kolom 'Gevraagde massa (gram)' in. We wilden weten hoeveel ijzeroxide nodig is voor 28 gram ijzer. Dus bij 'IJzer' in de kolom 'Gevraagde massa' vul je 28 in. De massa van ijzeroxide en zuurstof willen we berekenen; die blijven nog leeg of vul je in met een 'X' of vraagteken.
Stofnaam | Verhouding | Tussenstap | Gevraagde massa (gram) |
|---|---|---|---|
ijzeroxide | 7 | ||
ijzer | 5 | 28 | |
zuurstof | 2 |
Stap 5: De tussenstap gebruiken en doorrekenen
Nu gaan we rekenen! We gebruiken de 'Tussenstap' om van de verhouding naar de gevraagde massa te komen.
1.Kijk naar de stof waarvan je zowel de verhouding als de gevraagde massa weet (in dit geval ijzer).
2.Deel de verhouding door zichzelf om op '1' te komen in de kolom 'Tussenstap'. Voor ijzer is dat: 5 gram ÷ 5 = 1 gram.
3.Doe ditzelfde voor alle andere stoffen in de kolom 'Tussenstap':
•IJzeroxide: 7 gram ÷ 5 = 1,4 gram
•Zuurstof: 2 gram ÷ 5 = 0,4 gram
4.Kijk nu hoe je van '1' in de 'Tussenstap' naar de 'Gevraagde massa' komt. Voor ijzer is dat: 1 gram × 28 = 28 gram.
5.Doe ditzelfde voor de andere stoffen om hun gevraagde massa te berekenen:
•IJzeroxide: 1,4 gram × 28 = 39,2 gram
•Zuurstof: 0,4 gram × 28 = 11,2 gram
Stofnaam | Verhouding | Tussenstap | Gevraagde massa? |
|---|---|---|---|
ijzeroxide | 7 | 1,4 | 39,2 |
ijzer | 5 | 1 | 28 |
zuurstof | 2 | 0,4 | 11,2 |
Nu weet je dat je om 28 gram ijzer te maken, 39,2 gram ijzeroxide nodig hebt. Er ontstaat dan ook 11,2 gram zuurstof. En kijk: 39,2 gram (ijzeroxide) is precies 28 gram (ijzer) + 11,2 gram (zuurstof). De massa klopt weer!
Hoe weten fabrieken hoeveel materiaal ze nodig hebben?
Fabrieken maken veel producten, vaak met chemische reacties. Zij gebruiken precies deze manier van rekenen met verhoudingstabellen. Omdat de wet van behoud van massa altijd geldt (massa vóór een reactie is gelijk aan massa ná een reactie), kunnen ze nauwkeurig berekenen hoeveel van elk materiaal ze nodig hebben. Als een fabriek 1 kilogram van een product wil maken, weten ze dat ze in totaal 1 kilogram aan stoffen moeten gebruiken. Met de verhoudingstabel kunnen ze dan precies uitrekenen hoeveel ze van elke grondstof nodig hebben. Zo wordt er niks verspild en komt het eindproduct altijd perfect uit!














