Leg uit wat ontleden binnen scheikunde/NaSk2 betekent.
Leerdoelen
•Je kunt de drie typen ontledingsreacties benoemen.
•Je kunt uitleggen welke soort energie er nodig is voor elke specifieke ontledingsreactie.
•Je kunt stoffen indelen in ontleedbare stoffen en niet-ontleedbare stoffen.
Wat is ontleden?
Ontleden is het uit elkaar halen van moleculen. Moleculen kun je zien als kleine bouwwerkjes die bestaan uit nog kleinere onderdelen: atomen. Bij het ontleden haal je zo'n molecuul uit elkaar tot de losse atomen, net als wanneer je bouwstenen van elkaar losmaakt.
Om een stof te ontleden, heb je altijd energie nodig. Denk maar aan het loshalen van die bouwstenen; daar stop je ook kracht (energie) in. Deze energie kan verschillende vormen hebben. Een veelvoorkomende manier van ontleden is bijvoorbeeld door een stof te verhitten. De energievorm die je dan gebruikt, is warmte.

Ontledingsreacties
Je moet drie soorten ontledingsreacties kennen. Ze verschillen in de soort energie die ze nodig hebben.
Thermolyse: ontleden met warmte
Thermolyse komt van het woord 'thermo', wat warmte betekent. Dit is dus het ontleden van een stof met behulp van warmte. Je kunt dit doen door vuur tegen een stof aan te houden, de stof op een kookplaat te verwarmen of zelfs met een tosti-ijzer.
Elektrolyse: ontleden met elektriciteit
Bij elektrolyse gebruik je elektriciteit om een stof te ontleden. De naam 'elektrolyse' verraadt het al een beetje, want het lijkt op elektriciteit. Je laat dan stroom door de stof lopen. Een goed voorbeeld hiervan is het maken van waterstof. Waterstofauto's gebruiken waterstof om te rijden. Deze waterstof wordt gemaakt door water te ontleden met behulp van elektriciteit. Dit proces heet elektrolyse.
Fotolyse: ontleden met licht
Fotolyse is het ontleden van een stof met behulp van licht. Dit kan licht van een lamp zijn, maar ook gewoon licht van de zon. Een dagelijks voorbeeld zie je vaak bij posters die te lang buiten in de zon hangen. Ze worden dan helemaal bleek en de kleuren verdwijnen. Dit komt doordat het licht van de zon een chemische reactie veroorzaakt die de kleurstoffen in de poster ontleedt.
Ontleedbare en niet-ontleedbare stoffen
Niet alle stoffen kunnen zomaar ontleed worden. Sommige stoffen kunnen wel uit elkaar gehaald worden en andere niet.
Ontleedbare stoffen
Stoffen die je uit elkaar kunt halen, noemen we ontleedbare stoffen. Dit zijn alle stoffen die bestaan uit meerdere atomen of verschillende elementen. Denk aan water (H₂O), dat bestaat uit waterstofatomen (H) en zuurstofatomen (O). Water is een verbinding van meerdere atomen en kan gesplitst worden tot kleinere deeltjes (de losse atomen). Een molecuul is dus ontleedbaar als het kan worden gesplitst in kleinere, afzonderlijke atomen.
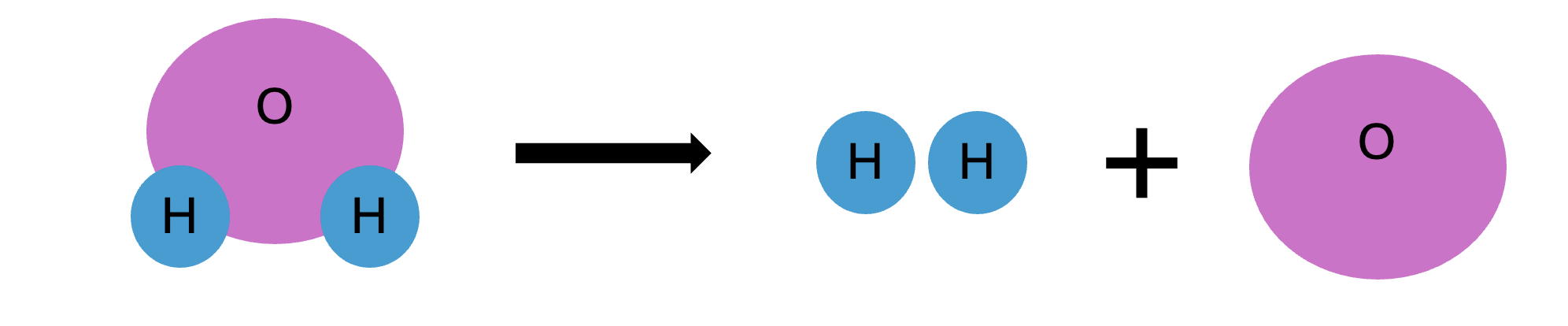
Niet-ontleedbare stoffen
Stoffen die niet verder uit elkaar gehaald kunnen worden, zijn niet-ontleedbare stoffen. Dit zijn de elementen zelf. Elementen zijn de kleinste stukjes materie die er bestaan en kunnen niet verder worden gesplitst in nog kleinere deeltjes. Een atoom van een element, zoals zuurstof (O) of ijzer (Fe), is dus niet-ontleedbaar.