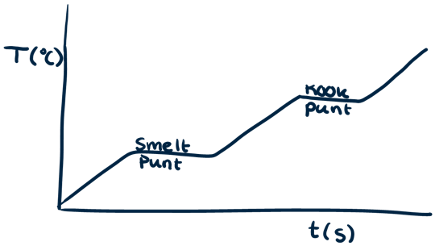
Welke drie fasen worden hier van links naar rechts aangegeven?
Leerdoelen
•Je kunt alle stofeigenschappen benoemen.
•Je kunt stofeigenschappen specifiek benoemen voor een bepaalde stof.
•Je kunt het kookpunt en smeltpunt herkennen in een temperatuur-tijdgrafiek.
•Je kunt de concentratie van een opgeloste stof berekenen.
De verschillende stofeigenschappen
Geur
De geur vertelt je hoe een stof ruikt. Ruikt het zoet, zuur, bitter of misschien helemaal nergens naar? Het is belangrijk om dit specifiek te benoemen. Je zegt niet "de citroen ruikt geur", maar "de citroen ruikt zuur". De geur van een citroen is dus zuur.
Kleur
De kleur is wat je ziet. Welke kleur heeft de stof? Let hierbij goed op, want je mag alleen kleuren benoemen die voorkomen in de regenboog of het kleurenspectrum. Goud, zilver en koper zijn geen kleuren. Goud is geel, zilver is grijs en koper is oranje. Schrijf dus bijvoorbeeld 'geel' op in plaats van 'goud'.

Smaak
De smaak beschrijft hoe een stof proeft. Smaakt het zoet, zuur, zout of bitter? Maar let op: in een scheikundelab mag je nooit zomaar iets proeven! Dit kan gevaarlijk zijn.

Brandbaarheid
Brandbaarheid geeft aan hoe goed een stof brandt. Vliegt het meteen in brand bij contact met vuur? Brandt het langzaam? Smelt het alleen? Of is het helemaal niet brandbaar en dus brandveilig?

Geleidbaarheid
De geleidbaarheid van een stof vertelt hoe goed stroom erdoorheen gaat. Geleidt de stof elektriciteit? Metalen, zoals koper, geleiden stroom vaak heel goed. Plastic geleidt daarentegen slecht; als je een lampje probeert aan te sluiten op plastic, zal het waarschijnlijk niet branden.

Kookpunt en smeltpunt
Het kookpunt en het smeltpunt zijn omslagpunten of faseovergangen. Dit zijn de temperaturen waarbij een stof verandert van de ene fase (vast, vloeibaar, gas) naar de andere. Water smelt bijvoorbeeld bij 0 graden Celsius (van ijs naar water) en kookt bij 100 graden Celsius (van water naar waterdamp).
Een faseovergang kost veel energie. Wanneer je een stof opwarmt, stijgt de temperatuur tot het smelt- of kookpunt is bereikt. Alle energie die je dan nog toevoegt, wordt gebruikt om de stof te laten smelten of koken. Pas als de hele stof van fase is veranderd, zal de temperatuur weer verder stijgen.
Kook- en smeltpunten herkennen in een grafiek
In een grafiek waar de temperatuur op de y-as en de tijd op de x-as staat, kun je het smelt- en kookpunt herkennen aan een horizontale lijn. De temperatuur blijft daar tijdelijk gelijk, terwijl er wel energie wordt toegevoegd (de tijd verstrijkt). Dit gebeurt omdat alle energie naar de faseovergang gaat.
Let op: deze horizontale lijnen zijn het duidelijkst bij zuivere stoffen. Bij mengsels zijn ze vaak minder strak horizontaal, maar nog steeds herkenbaar als een 'bijna' horizontale lijn. Je kunt deze punten aflezen uit een grafiek, opzoeken in een tabel (bijvoorbeeld in de Binas) of soms weet je ze al uit je hoofd.
Dichtheid
De dichtheid vertelt hoeveel stof er in een bepaald volume past. Elke stof heeft zijn eigen unieke dichtheid. Goud heeft bijvoorbeeld een andere dichtheid dan ijzer of water. De formule om dichtheid te berekenen is: dichtheid = massa / volume De dichtheid van een stof kun je vinden in tabellen in je boek of in de Binas. Je moet dan goed kijken of het gaat om de dichtheid van vaste stoffen, vloeistoffen of gassen.
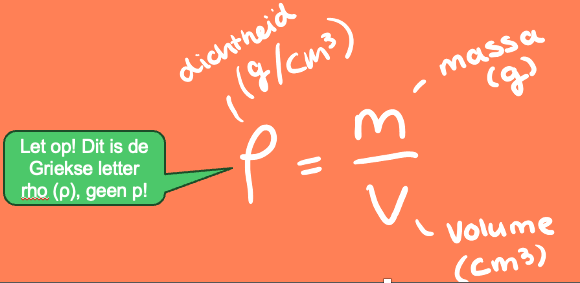
Fase bij kamertemperatuur
Dit is een stofeigenschap die aangeeft in welke fase (vast, vloeibaar of gas) een stof zich bevindt bij kamertemperatuur (ongeveer 20 graden Celsius). Water is bijvoorbeeld vloeibaar bij kamertemperatuur, terwijl suiker vast is (korreltjes).
Oplosbaarheid en concentratie
Oplosbaarheid
De oplosbaarheid geeft aan hoe goed een stof oplost in een andere stof, meestal een vloeistof. Als je suiker in water doet, lost het op en verdwijnt het.
Concentratie berekenen
Als een stof is opgelost, kun je de concentratie ervan berekenen. Dit vertelt je hoeveel van de stof is opgelost in een bepaalde hoeveelheid vloeistof. De formule hiervoor lijkt op die van dichtheid: concentratie = massa opgeloste stof / volume oplosmiddel
Hier zijn twee rekenvoorbeelden:
1.Stel, je lost 2 gram suiker op in 1 liter water. De concentratie is dan: concentratie = 2 gram / 1 liter = 2 gram per liter (2 g/L).
2.Als je 10 gram suiker in 2 liter water doet, is de concentratie: concentratie = 10 gram / 2 liter = 5 gram per liter (5 g/L). Het oplosmiddel is de vloeistof waarin je de stof oplost, in deze voorbeelden is dat water.
Voorbeeld van herkennen aan de hand van stofeigenschappen
Hoe kan je bepalen dat de witte korrels in je bakje suiker zijn? Dit kan door alle stofeigenschappen af te gaan:
•Kleur: suiker is wit of een beetje doorzichtig.
•Geur: suiker ruikt naar niks, of soms heel licht zoet.
•Smaak: suiker smaakt zoet (maar vergeet de waarschuwing over proeven niet!).
•Brandbaarheid: als je suiker verwarmt, smelt het en wordt het karamel. Het vliegt dus niet zomaar in brand.
•Geleidbaarheid: suiker geleidt geen elektriciteit. Een lampje zal niet branden als je het aansluit op suiker.
•Smeltpunt: het smeltpunt van suiker ligt rond de 160 graden Celsius. Dit kun je opzoeken.
•Oplosbaarheid: suiker is goed oplosbaar in water. Het verdwijnt als je het erin doet.
•Dichtheid: suiker heeft een specifieke dichtheid die je kunt meten of opzoeken.
•Fase bij kamertemperatuur: suiker is een vaste stof bij kamertemperatuur (korreltjes).
Met al deze stofeigenschappen kun je bepalen of de stof in het potje inderdaad suiker is.














