Leg in één zin uit wat een molecuulformule laat zien
Leerdoelen
•Je kunt een molecuulformule opstellen.
•Je kunt verschillende molecuulformules benoemen.
•Je kunt het verschil uitleggen tussen een reactieschema en een reactievergelijking.
•Je kunt een reactieschema opstellen.
•Je kunt een reactievergelijking opstellen en kloppend maken.
Molecuulformules: de bouwstenen van reacties
Een molecuulformule laat zien hoeveel en welke atomen er in een molecuul zitten. Dit doen we met behulp van de chemische symbolen (de afkortingen van atomen, zoals H voor waterstof en O voor zuurstof) en getallen. Deze getallen noemen we een index en ze staan heel klein rechtsonder het symbool van het atoom. Ze geven aan hoe vaak dat atoom in het molecuul voorkomt. Als een atoom maar één keer voorkomt, schrijven we de index 1 niet op.
Voorbeeld: Water bestaat uit twee waterstofatomen en één zuurstofatoom.
Het symbool voor waterstof is H. Omdat er twee waterstofatomen zijn, krijgt H een index 2: .
Het symbool voor zuurstof is O. Omdat er één zuurstofatoom is, schrijven we alleen O (de index 1 hoeft niet). De molecuulformule voor water is dus .
Belangrijke molecuulformules om te kennen
Sommige molecuulformules is het handig om uit je hoofd te kennen, omdat ze vaak voorkomen in scheikunde en soms niet in je Binas staan. In elk NaSk-boek staat meestal een tabel met deze veelvoorkomende formules. Denk aan stoffen als alcohol, ammoniak, glucose (), methaan, soda, water en waterstofperoxide.
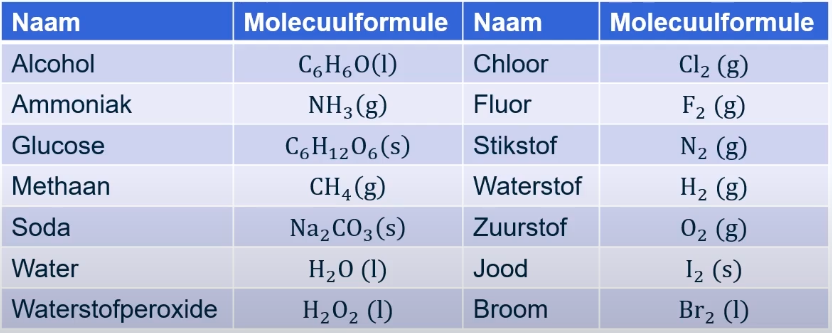
Elementen die altijd twee-atomig voorkomen
Een speciale groep elementen komt in de natuur nooit als los atoom voor. Ze zijn altijd verbonden met een ander atoom, vaak met een ander atoom van dezelfde soort. Ze vormen dan een molecuul met z'n tweeën. Dit zijn er zeven: chloor (Cl), fluor (F), stikstof (N), waterstof (H), zuurstof (O), jood (I) en broom (Br).
Dus, als je deze stoffen in hun pure vorm tegenkomt, schrijf je hun molecuulformule met een index 2: , , , , , , .
Ezelsbruggetje om te onthouden: "Claire fietst naar haar oma in Breda"
Claire (Chloor, )
Fietst (Fluor, )
Naar (Stikstof, )
Haar (Waterstof, )
Oma (Zuurstof, )
In (Jood, )
Breda (Broom, )
Dit is erg belangrijk als je reactievergelijkingen gaat opstellen. Als zuurstof bijvoorbeeld deel uitmaakt van een verbrandingsreactie, moet je altijd gebruiken, niet alleen O.
Van reactieschema naar kloppende reactievergelijking
We kunnen een chemische reactie op verschillende manieren opschrijven.
Reactieschema
Een reactieschema beschrijft een reactie in woorden. Je gebruikt de stofnamen van de beginstoffen (voor de pijl) en de reactieproducten (na de pijl).
Voorbeeld: Methaan koolstof + waterstof. Hier is 'methaan' de beginstof, en 'koolstof' en 'waterstof' zijn de reactieproducten.
Reactievergelijking
Een reactievergelijking is de wiskundige manier om een reactie weer te geven. Hierin gebruik je geen woorden, maar molecuulformules (symbolen met indexgetallen). Bij een reactievergelijking moet het aantal atomen van elke soort voor de pijl precies gelijk zijn aan het aantal atomen van elke soort na de pijl. Dit noemen we het kloppend maken van de reactievergelijking.
Voorbeeld: Methaan wordt koolstof en waterstof
Reactieschema: Methaan koolstof + waterstof
Reactievergelijking:
In een reactievergelijking voegen we ook de fase van de stof toe, tussen haakjes achter de molecuulformule:
(g) voor gas
(l) voor vloeibaar (liquid)
(s) voor vast (solid)
(aq) voor opgelost in water (aqueous)
Voorbeeld met fases:
Om een reactievergelijking kloppend te maken, gebruiken we een coëfficiënt. Dit is een groot getal dat vóór de hele molecuulformule van een stof staat. Het geeft aan hoeveel moleculen van die stof je nodig hebt.
Index: klein getal rechtsonder, geeft aan hoeveel atomen er in één molecuul zitten (bijv. de '2' in ).
Coëfficiënt: groot getal voor de formule, geeft aan hoeveel moleculen er nodig zijn (bijv. de '2' in ).
Oefening: een reactievergelijking kloppend maken
Laten we oefenen met het kloppend maken van de reactie van methaan die koolstof en waterstof vormt:
Reactievergelijking (niet kloppend):
Tel de atomen voor en na de pijl:
C-atomen:Voor de pijl (in ): 1 CNa de pijl (in C): 1 CDe C-atomen kloppen al.
H-atomen:Voor de pijl (in ): 4 H (door de index 4)Na de pijl (in ): 2 H (door de index 2)De H-atomen kloppen niet; er zijn te weinig H-atomen na de pijl.
Maak de H-atomen kloppend:
We hebben 4 H-atomen voor de pijl en 2 H-atomen na de pijl. Om van 2 naar 4 te komen, moeten we de na de pijl vermenigvuldigen met 2. Dit doen we door een coëfficiënt 2 voor te plaatsen.
De vergelijking wordt:
Controleer alle atomen opnieuw:
C-atomen:Voor de pijl (in ): 1 CNa de pijl (in C): 1 CKlopt.
H-atomen:Voor de pijl (in ): 4 HNa de pijl (in ): 2 (coëfficiënt) (index) = 4 HKlopt.
De kloppende reactievergelijking is:
Stap voor stap: verbranding van buteen kloppend maken
Laten we een uitgebreider voorbeeld doen: de verbranding van buteen.
Gegeven: Bij de verbranding van buteen () ontstaan koolstofdioxide en water. Maak een kloppende reactievergelijking.
Stap 1: Maak een reactieschema
"Verbranding" betekent dat zuurstof () een van de beginstoffen is.
De beginstoffen zijn dus buteen en zuurstof.
De reactieproducten zijn koolstofdioxide en water.
Reactieschema: buteen + zuurstof koolstofdioxide + water
Stap 2: Vervang woorden door molecuulformules en voeg fases toe
Buteen: (gas, g)
Zuurstof: (gas, g) (denk aan het ezelsbruggetje!)
Koolstofdioxide: (gas, g)
Water: (vloeibaar, l)
Reactievergelijking (niet kloppend):
Stap 3: Maak de hoeveelheden kloppend (tellen en aanpassen) We tellen de atomen voor en na de pijl. Het is handig om eerst de C- en H-atomen kloppend te maken, en de O-atomen als laatste, omdat zuurstof als voorkomt en je die makkelijk kunt aanpassen.
Beginstand:
C: 4 (voor pijl in ), 1 (na pijl in )
H: 8 (voor pijl in ), 2 (na pijl in )
O: 2 (voor pijl in ), 3 (na pijl: 2 in + 1 in )
Maak de H-atomen kloppend:
Voor de pijl 8 H, na de pijl 2 H. We moeten de H-atomen na de pijl keer 4 doen.
Plaats een coëfficiënt 4 voor
Tel opnieuw na aanpassing H:
C: 4 (voor), 1 (na)
H: 8 (voor), 8 (na: KLOPT
O: 2 (voor), 6 (na: 2 in 1 in )
Maak de C-atomen kloppend:
Voor de pijl 4 C, na de pijl 1 C. We moeten de C-atomen na de pijl keer 4 doen.
Plaats een coëfficiënt 4 voor
Tel opnieuw na aanpassing C:
C: 4 (voor), 4 (na) KLOPT
H: 8 (voor), 8 (na) KLOPT
O: 2 (voor), 12 (na: 4 1 in )
Maak de O-atomen kloppend:
Voor de pijl 2 O, na de pijl 12 O. We moeten de O-atomen voor de pijl keer 6 doen.
Plaats een coëfficiënt 6 voor
Laatste controle van alle atomen:
C-atomen:Voor de pijl (in ): 4 CNa de pijl (in ): 4 CKLOPT.
H-atomen:Voor de pijl (in ): 8 HNa de pijl (in ): 2 = 8 HKLOPT.
O-atomen:Voor de pijl (in ): 6 2 = 12 ONa de pijl (in ) = 8 + 4 = 12 OKLOPT.
De kloppende reactievergelijking voor de verbranding van buteen is dus:














