Uit welke drie deeltjes is een atoom opgebouwd?
Leerdoelen
•Je kunt de drie deeltjes benoemen waaruit een atoom is opgebouwd.
•Je kunt uitleggen wat atoommassa is en de bijbehorende eenheid benoemen.
•Je kunt uitleggen wat het massagetal is en dit berekenen voor een gegeven atoom.
•Je kunt uitleggen waarom elektronen niet meetellen in het massagetal.
Het atoom
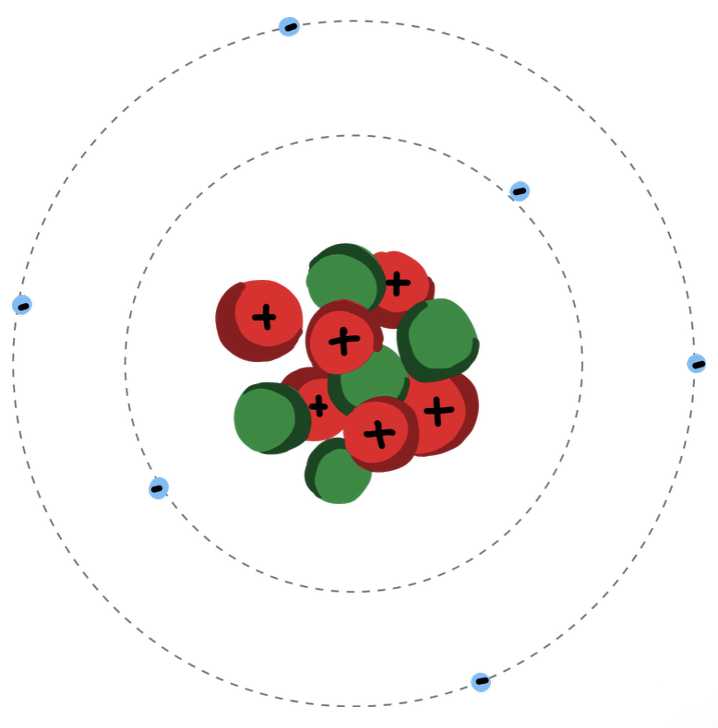
In het midden van een atoom zit de atoomkern. Dit is het hart van het atoom. In de kern vind je twee soorten deeltjes:
•Protonen: Dit zijn positief geladen deeltjes. We geven ze vaak aan met een plusje (+). De lading van een proton is +1.
•Neutronen: Deze deeltjes zijn neutraal, ze hebben geen lading. Je kunt ze zien als de 'lijm' die de protonen bij elkaar houdt in de kern.
Om de atoomkern heen zweeft een elektronenwolk. In dit gebied bewegen de nog kleinere deeltjes:
•Elektronen: Dit zijn negatief geladen deeltjes. We geven ze vaak aan met een minnetje (-). De lading van een elektron is -1.
De lading van een proton (+1) en een elektron (-1) zijn even groot, maar tegenovergesteld. Stel je voor dat je zes protonen hebt (+6) en zes elektronen (-6). De totale lading is dan nul, omdat de positieve en negatieve ladingen elkaar opheffen:+6-6=0\left(+6-6=0\right.\left(+6-6=0\right). Zo'n atoom noemen we een elektrisch neutraal atoom. Het heeft dan geen totale lading.
Het atoomnummer
Elk atoom heeft een uniek nummer: het atoomnummer. Dit nummer wordt bepaald door het aantal protonen in de kern. Als je het aantal protonen telt, dan weet je het atoomnummer. Let op: De kleur of het symbool kan op verschillende tekeningen anders zijn, dus let goed op de plusjes (+) om protonen te herkennen.
In de afbeelding van ons atoom tellen we zes rode bolletjes met een plusje, dus zes protonen. Het atoomnummer is dan zes. Het atoomnummer staat altijd linksboven in het vakje van een element in het periodiek systeem (ook te vinden in je Binas).

Als je weet dat het atoomnummer zes is, kun je in het periodiek systeem opzoeken dat dit atoom koolstof is. Als dit koolstofatoom elektrisch neutraal is, dan moet het net zoveel elektronen als protonen hebben. Aangezien het zes protonen heeft, heeft het ook zes elektronen.
Atoommassa
Alle deeltjes in een atoom hebben massa. Samen bepalen ze de massa van het hele atoom. De atoommassa is de werkelijke, precieze massa van een atoom. Maar de massa van deze deeltjes is zó ongelooflijk klein, dat het onhandig zou zijn om ze in kilogram (kg) uit te drukken. Je zou dan met getallen als 0,0000000000000000000000000017 kg moeten werken. Dit maakt rekenen moeilijk en de kans op fouten groter.
Daarom is er een speciale eenheid bedacht voor de massa van atomen: de universele atomaire massa-eenheid, afgekort u. Eén u is ongeveer gelijk aan. Gelukkig hoef je dit getal niet te onthouden. Het belangrijkste is dat rekenen met 'u' veel makkelijker is.
Deeltje | Massa (u) |
|---|---|
Proton | 1 |
Neutron | 1 |
Elektron | 0,00055 |
Je ziet dat de massa van een elektron heel erg klein is vergeleken met die van een proton of een neutron.
Het massagetal
Het massagetal is de som van het aantal deeltjes in de atoomkern (protonen en neutronen).
Elektronen worden niet meegeteld, omdat de massa van een elektron (0,00055 u) zo ontzettend klein is dat deze te verwaarlozen is. Het heeft bijna geen invloed op de totale massa van het atoom. Het is alsof je probeert het gewicht van een vrachtwagen te bepalen, en je vraagt je af of een klein vliegje dat erop zit meetelt. De bijdrage is veel te klein en het is makkelijker rekenen zonder die mee te tellen.
Laten we het massagetal berekenen voor ons voorbeeldatoom, dat zes protonen en vijf neutronen heeft:
•Aantal protonen: 6
•Aantal neutronen: 5
•\text{massagetal }=6+5=11\text{massagetal }=6+5=11\text{ }
Dit betekent dat de massa van dit specifieke koolstofatoom ongeveer 11 u is. Het massagetal is dus een benadering van de atoommassa, uitgedrukt in u.














