Mees verwarmt water en het water bereikt het kookpunt. Mees laat het fornuis aanstaan. Wat gebeurt er met de temperatuur van het water?
Leerdoelen
•Je kunt uitleggen wat er gebeurt als water kookt.
•Je kunt de begrippen kookpunt, smeltpunt, vriespunt en stolpunt uitleggen.
•Je kunt beschrijven hoe je kookpunten en stolpunten kunt beïnvloeden.
•Je kunt smelt- en stollingsdiagrammen van een zuivere stof aflezen.
•Je kunt smelt- en stollingsdiagrammen van een mengsel aflezen.
Het kookpunt
Het kookpunt is de temperatuur waarbij een zuivere stof verandert van een vloeistof naar een gas. Een zuivere stof bestaat uit één soort moleculen. Deze verandering noemen we verdampen.
Voor water is het kookpunt precies100\degree\text{C}100\degree100\degree100\degree100\degree100\degree100\degree100\degree100\degree100\degree100100100100100100\degree. Dit betekent dat bij100\degree\text{C}al het water bezig is om te verdampen en waterdamp te worden. Deze snelle vorm van verdampen, die door de hele vloeistof heen gebeurt, noemen we koken. Het verschil tussen verdampen en koken is dat verdampen aan het oppervlak plaatsvindt bij elke temperatuur tussen het smeltpunt en het kookpunt, terwijl koken in de hele vloeistof gebeurt en alleen bij het kookpunt. Tijdens het koken blijft de temperatuur van het water100\degree\text{C}, ook als je energie blijft toevoegen. Pas als al het water is verdampt, kan de temperatuur van de waterdamp verder stijgen.
Smeltpunt, stolpunt en vriespunt
Naast het kookpunt zijn er nog andere belangrijke temperaturen die aangeven wanneer een stof van fase verandert.
Het smeltpunt is de temperatuur waarbij een zuivere stof verandert van een vaste stof naar een vloeistof. Dit proces heet smelten. Neem bijvoorbeeld ijs. IJs is de vaste vorm van water. Het smeltpunt van water is0\degree\text{C}10\degree\text{C}100\degree\text{C}. Bij deze temperatuur begint ijs te smelten en verandert het in vloeibaar water. Voor een zuivere stof liggen het smeltpunt en het stolpunt altijd op dezelfde temperatuur.
Het stolpunt is de temperatuur waarbij een zuivere stof verandert van een vloeistof naar een vaste stof. Dit proces noemen we stollen. Specifiek voor water gebruiken we de term bevriezen en noemen we het bijbehorende punt het vriespunt. Alleen bij water spreken we van bevriezen; bij andere stoffen noemen we het altijd stollen. Water bevriest ook bij0\degree\text{C}0\text{C}0\text{C}0\circ\text{C}0\text{C}0\text{C}0\text{C}0\text{C}0\text{C}0\degree\text{C}10\degree\text{C}100\degree\text{C}. Dus als vloeibaar water afkoelt tot0\degree\text{C}10\degree\text{C}100\degree\text{C}, zal het stollen en ijs worden.
Kook- en smeltpunten zijn stofeigenschappen
Het kookpunt en smeltpunt van een zuivere stof zijn unieke eigenschappen van die stof. Ze zijn als een vingerafdruk. Water heeft bijvoorbeeld een smeltpunt van0\degree\text{C}10\degree\text{C}100\degree\text{C}en een kookpunt van100\degree\text{C}. Aan deze unieke waarden kun je de stof herkennen.
Kook- en smeltpunten beïnvloeden
Door een andere stof aan een zuivere stof toe te voegen, maak je een mengsel. Hiermee kun je het kook- en smeltpunt beïnvloeden. Denk bijvoorbeeld aan het toevoegen van zout aan water.
Het toevoegen van zout aan water verhoogt het kookpunt en verlaagt het smelt- en vriespunt. Dit betekent dat zout water warmer kan worden voordat het kookt, en kouder kan worden voordat het bevriest. Daarom wordt er in de winter zout op de wegen gestrooid. Het zout zorgt ervoor dat water op de weg minder snel bevriest, waardoor de wegen minder glad zijn. Een ander voorbeeld is het toevoegen van zout aan het kookwater van pasta. Hoewel de invloed op het kookpunt klein is, zorgt het zout ervoor dat de pasta op een iets hogere temperatuur kookt.
Diagrammen
Deze faseovergangen kun je goed laten zien in speciale grafieken die we smelt- en stollingsdiagrammen noemen.
Diagram van een zuivere stof
In een diagram van een zuivere stof zie je dat de temperatuur eerst stijgt. Maar op het moment dat de stof begint te smelten of te koken, zie je een horizontale lijn. Dit komt omdat alle energie die je toevoegt, dan wordt gebruikt om de faseovergang te laten plaatsvinden. De temperatuur van de stof stijgt of daalt dan niet. Je kunt aan deze horizontale lijnen precies aflezen wat het smeltpunt en het kookpunt van de stof zijn.
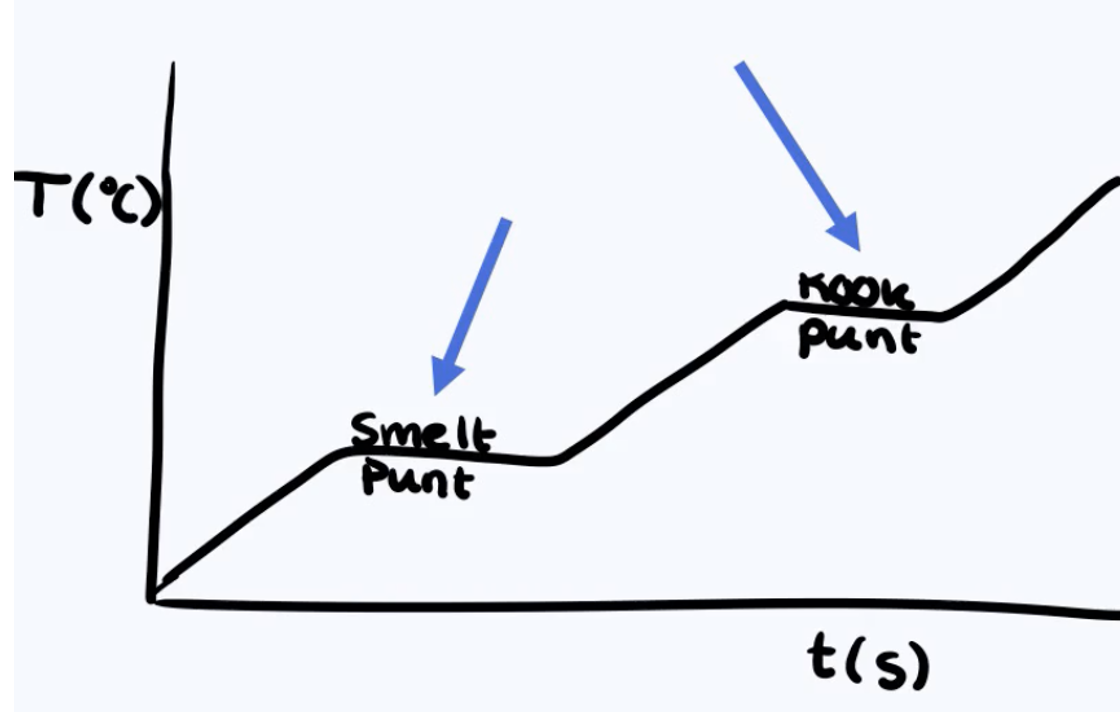
Hetzelfde geldt bij het afkoelen: tijdens het condenseren en stollen blijft de temperatuur ook constant, wat te zien is als een horizontale lijn in een diagram.
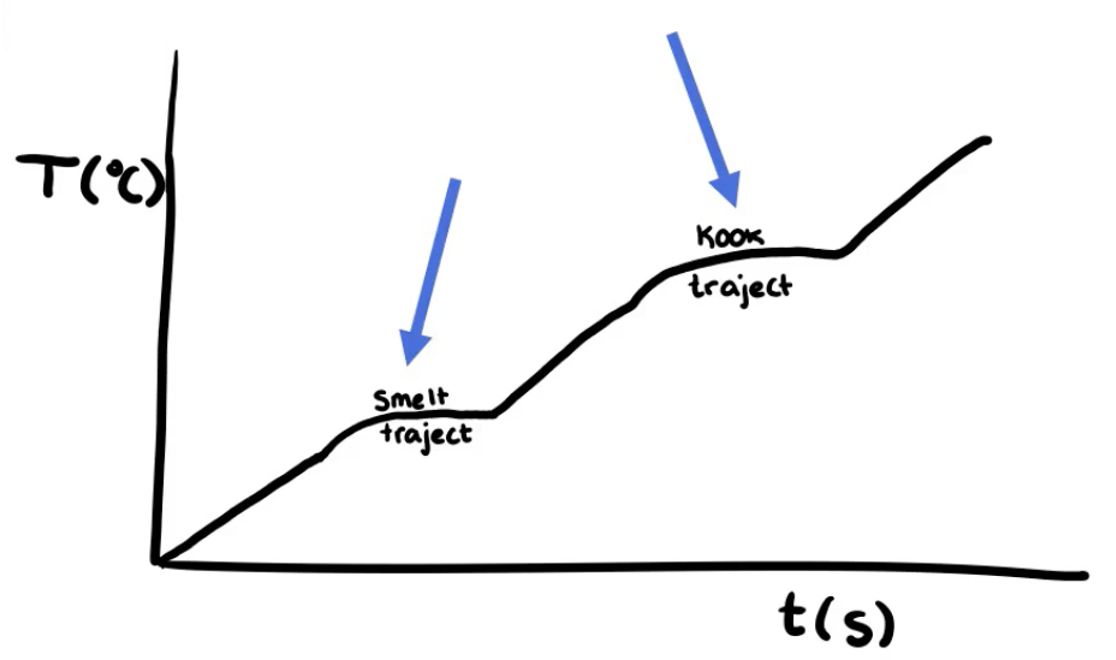
Diagram van een mengsel
Omdat mengsels uit meerdere soorten moleculen bestaan, hebben ze niet één precies punt waarop de faseovergang plaatsvindt. In plaats van een horizontale lijn zie je tijdens de faseovergang een schuin oplopend stuk in het diagram. De temperatuur blijft dus stijgen, maar minder snel dan daarvoor. Dit noemen we geen punten, maar trajecten. Bij opwarmen spreken we van een smelttraject en een kooktraject, en bij afkoelen van een stoltraject. De faseovergang vindt dan plaats over een bepaald temperatuurbereik in plaats van op één specifieke temperatuur.