Noteer bij elk nummer de juiste stofeigenschap.
Leerdoelen
•Je kunt alle stofeigenschappen benoemen
•Je kunt stofeigenschappen voor een specifieke stof benoemen
•Je kunt het kookpunt en smeltpunt in een grafiek herkennen
•Je kunt de concentratie van een stof berekenen
De zichtbare en meetbare eigenschappen
Er zijn veel verschillende soorten stofeigenschappen. We gaan ze één voor één langs.
Geur
Hoe ruikt een stof? Iets kan zoet ruiken of juist zuur.

Kleur
Welke kleur heeft een stof? Dit is een eigenschap die je kunt zien. Let goed op: je mag alleen kleuren gebruiken die in de regenboog of het spectrum voorkomen. "Goud", "zilver" en "koper" zijn geen kleuren! Koper is oranje, goud is geel en zilver is grijs.

Smaak
Hoe smaakt een stof? Dit kun je proeven. Let op: in een scheikundelokaal mag je nooit zomaar een stof proeven, omdat dit gevaarlijk kan zijn!

Brandbaarheid
Hoe goed brandt een stof? Sommige stoffen vliegen direct in brand wanneer je er vuur bij houdt. Andere branden langzaam, smelten eerst, of branden helemaal niet. Een stof die niet brandt, is brandveilig.

Geleidbaarheid
Hoe goed gaat stroom door een stof heen? Dat noemen we geleidbaarheid. Geleidt de stof elektriciteit? Metalen, zoals koperdraadjes, laten stroom vaak goed door en geleiden dus goed. Plastic daarentegen geleidt slecht; als je een lampje op plastic aansluit, zal het niet gaan branden.

Kookpunt en smeltpunt: de faseovergangen
Het kookpunt en smeltpunt zijn belangrijke stofeigenschappen die aangeven wanneer een stof van de ene naar de andere fase overgaat. Dit worden ook wel faseovergangen genoemd.
Wat zijn kookpunt en smeltpunt?
Water is een goed voorbeeld:
•Water gaat van vast (ijs) naar vloeibaar (water) bij 0 graden Celsius. Dit is het smeltpunt. Hier smelt het water.
•Water gaat van vloeibaar (water) naar gas (waterdamp) bij 100 graden Celsius. Dit is het kookpunt. Hier gaat het water koken.
Een faseovergang kost veel energie. Wanneer je een stof opwarmt, wordt deze eerst warmer. Maar zodra de stof het smelt- of kookpunt bereikt, gaat alle toegevoegde energie eerst naar de faseovergang (smelten of koken) voordat de stof weer verder kan opwarmen.
Kook- en smeltpunt in een grafiek
Door deze energiebehoefte voor faseovergangen ziet een grafiek van temperatuur tegen tijd er op een speciale manier uit.
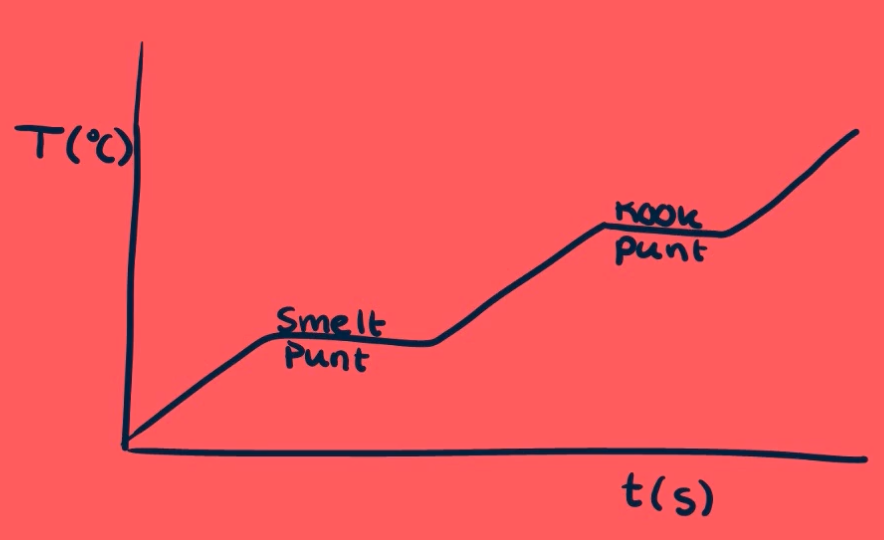
Je stopt energie in de stof (bijvoorbeeld door te verwarmen), dus de temperatuur stijgt. Maar wanneer de stof het smeltpunt bereikt, zie je dat de lijn horizontaal wordt. Alle energie gaat nu naar het smelten van de stof, en de temperatuur blijft constant totdat de hele stof gesmolten is. Pas daarna kan de temperatuur weer verder stijgen. Hetzelfde gebeurt bij het kookpunt.
In zo'n grafiek herken je het kookpunt en het smeltpunt dus aan de horizontale lijnen. Let op: dit geldt vooral voor zuivere stoffen. Bij mengsels zien de lijnen er iets minder horizontaal uit, maar zijn ze nog steeds herkenbaar als bijna horizontale stukken.
Je kunt het kookpunt en smeltpunt aflezen uit een grafiek, opzoeken in een tabel (bijvoorbeeld de Binas), of soms weet je ze gewoon al (zoals bij water).
Dichtheid: hoe compact is een stof?
De dichtheid vertelt je hoeveel massa van een stof er past in een bepaald volume. Gouden voorwerpen voelen bijvoorbeeld veel zwaarder aan dan ijzeren voorwerpen van dezelfde grootte, omdat goud een hogere dichtheid heeft.
De formule om dichtheid te berekenen is: dichtheid = massa / volume
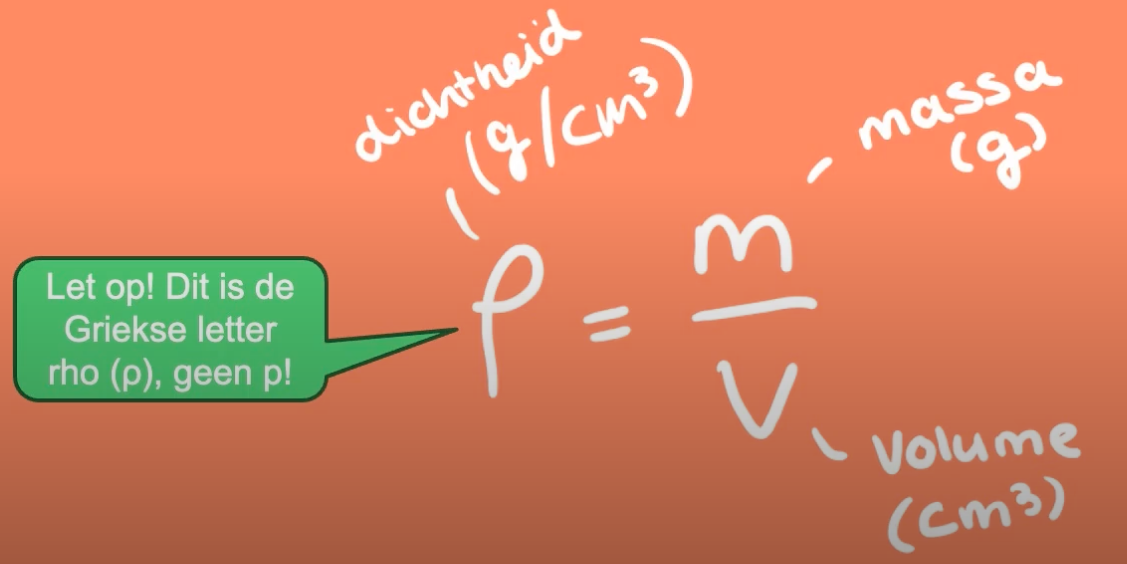
Iedere stof heeft zijn eigen unieke dichtheid. Goud heeft een andere dichtheid dan ijzer, en ijzer heeft weer een andere dichtheid dan water. De dichtheid van stoffen kun je vinden in tabellen in je boek of in de Binas. Je moet dan kijken bij de dichtheid van vaste stoffen, vloeistoffen of gassen.
Fase bij kamertemperatuur
Alle stoffen bevinden zich in een bepaalde fase (vast, vloeibaar of gas) bij kamertemperatuur. De kamertemperatuur is ongeveer 20 graden Celsius. Je kunt deze stofeigenschap beschrijven door te zeggen of iets vast, vloeibaar of gas is bij die temperatuur. Water is bij kamertemperatuur vloeibaar, terwijl suiker vast is (het zijn korreltjes).
Oplosbaarheid en concentratie
Twee andere belangrijke stofeigenschappen zijn oplosbaarheid en concentratie.
Oplosbaarheid
De oplosbaarheid van een stof geeft aan hoe goed de stof oplost in een vloeistof. Losse korrels suiker bijvoorbeeld, zijn goed oplosbaar in water.
Concentratie berekenen
Als een stof eenmaal is opgelost, kun je iets zeggen over de concentratie van de stof. De concentratie geeft aan hoeveel van de stof is opgelost in een bepaalde hoeveelheid vloeistof.
Je kunt de concentratie berekenen met een formule die lijkt op die van de dichtheid: concentratie = massa van de stof (m) / volume van het oplosmiddel (V): C=\frac{m}{V}C=\frac{m}{V}VC=\frac{m}{\placeholder{}}VC=mV
Het oplosmiddel is de vloeistof waarin je de stof oplost. Als je suiker in water oplost, is water het oplosmiddel.
Rekenvoorbeelden:
Stel, je lost 2 gram suiker op in 1 liter water. De concentratie is dan: 2 gram / 1 liter = 2 gram per liter (2 g/L).
Stel, je lost 10 gram suiker op in 2 liter water. De concentratie is dan: 10 gram / 2 liter = 5 gram per liter (5 g/L).














