Noem de drie verschillende fasen waarin stoffen kunnen voorkomen.
Leerdoelen
•Je kunt uitleggen wat moleculen zijn
•Je kunt uitleggen in welke 3 fases stoffen voorkomen
•Je kunt uitleggen wat er gebeurt bij uitzetten en krimpen
•Je kunt alle faseovergangen benoemen
Wat zijn moleculen?
Moleculen zijn de kleine deeltjes waaruit stoffen bestaan. Als je bijvoorbeeld inzoomt op een glas water, zie je dat het uit watermoleculen bestaat. Deze moleculen zijn altijd in beweging, al is het maar een klein beetje. Hoe die moleculen bewegen en op welke plek ze zitten bepaalt de fase van een stof. Er zijn drie verschillende fase waarin stoffen kunnen voorkomen: vast, vloeibaar en gas.
Vaste fase
In de vaste fase zitten moleculen op een vaste plek en trillen lichtjes. Dit kan je vergelijken met leerlingen die bij een schoolfeest langs de rand staan en nauwelijks bewegen.
Vloeibare fase
In de vloeibare fase bewegen moleculen iets meer en hebben dan ook meer ruimte nodig. Dit is vergelijkbaar met leerlingen die op de dansvloer bij een schoolfeest staan en een beetje dansen.
Gasfase
In de gasfase bewegen moleculen vrij en hebben ze veel ruimte nodig. Dit zijn dan de leerlingen op het schoolfeest die overal dansen en veel ruimte innemen.

Uitzetten en krimpen
Wanneer de temperatuur stijgt, krijgen moleculen meer energie en gaan ze meer bewegen. Hierdoor hebben ze meer ruimte nodig en zet het materiaal uit. Dit proces heet uitzetten. Het tegenovergestelde gebeurt bij krimpen: als de temperatuur daalt, verliezen moleculen energie, bewegen ze minder en hebben ze minder ruimte nodig.
Een voorbeeld hiervan is het ontploffen van een fietsband als hij te lang in de zon staat. De zwarte kleur van de band absorbeert veel energie, waardoor de temperatuur stijgt. De moleculen in de lucht binnenin de band krijgen meer energie, bewegen meer en hebben meer ruimte nodig. Hierdoor zet de lucht uit. Als de druk te hoog wordt, kan de band het niet meer aan en ontploft hij.
Faseovergangen
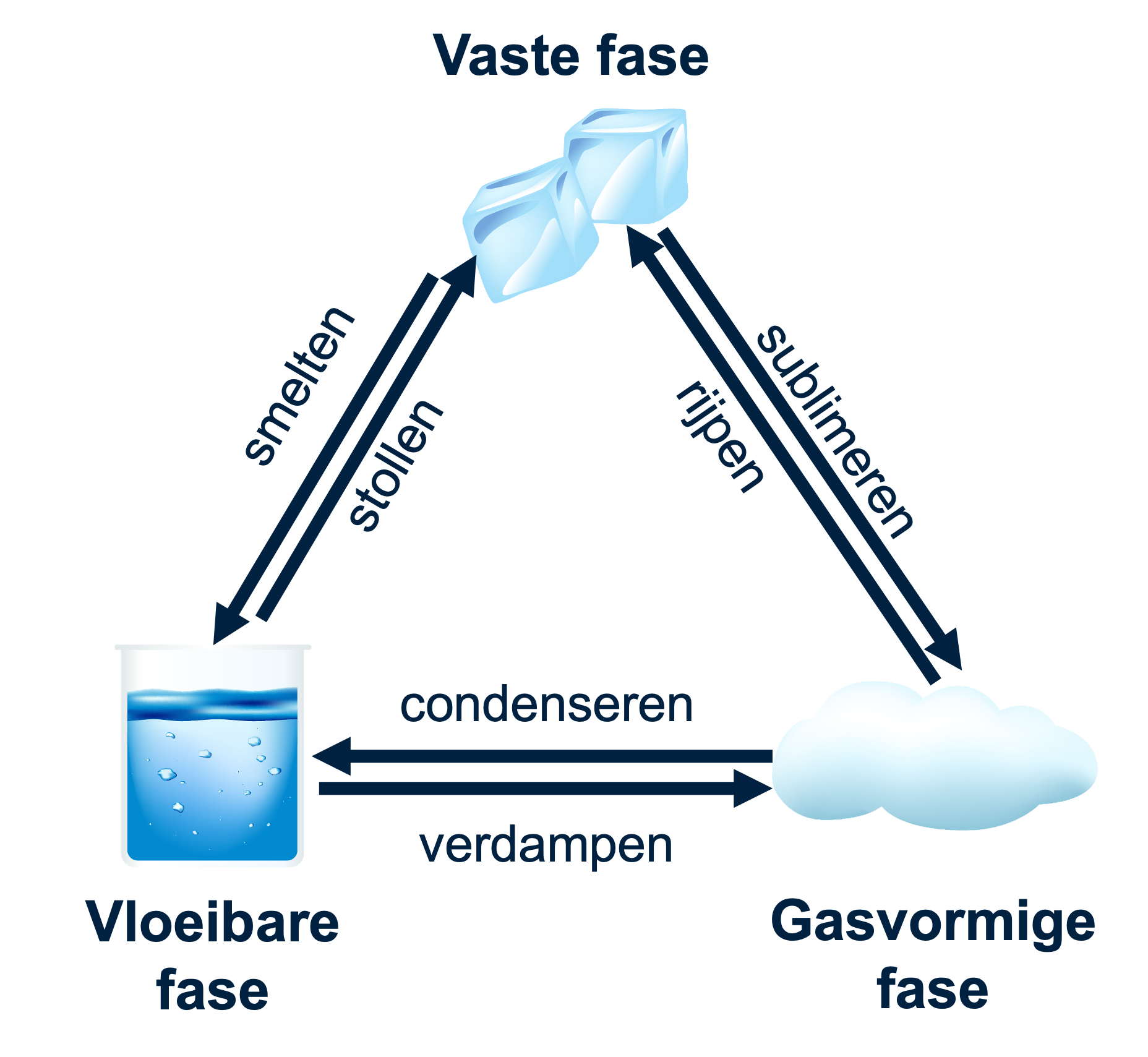
Wanneer de temperatuur in extreme mate stijgt of daalt, vindt er een faseovergang plaats. Er zijn zes belangrijke faseovergangen:
•Smelten: vaste stof wordt vloeibaar
•Stollen: vloeibare stof wordt vast
•Verdampen: vloeibare stof wordt gas
•Condenseren: gas wordt vloeibaar
•Sublimeren: vaste stof wordt gas
•Rijpen: gas wordt vast