Wat gebeurt er met de Van der Waals kracht en -binding als de massa van een molecuul groter is?
Leerdoelen
•Je kunt uitleggen wat de kapstok van de scheikunde is.
•Je kunt uitleggen wat de vanderwaalskracht is.
•Je kunt uitleggen wat de vanderwaalsbinding is.
De kapstok van de scheikunde
Voordat we dieper ingaan op de vanderwaalsbindingen, frissen we eerst de basis van de scheikunde op. Stoffen kunnen we indelen in drie hoofdcategorieën:
•Metalen: dit zijn elementen die alleen uit metaalatomen bestaan, zoals ijzer (Fe) of koper (Cu).
•Zouten: deze stoffen bestaan uit een combinatie van metaalatomen en niet-metaalatomen, zoals natriumchloride (NaCl).
•Moleculaire stoffen: deze stoffen bestaan uitsluitend uit niet-metaalatomen, zoals water (H₂O) of koolstofdioxide (CO₂).

De vanderwaalskracht en -binding
Moleculen, de bouwstenen van moleculaire stoffen, trekken elkaar aan. Dit komt doordat ze massa hebben. Net zoals de aarde en de zon elkaar aantrekken door hun massa, oefenen moleculen ook een aantrekkingskracht op elkaar uit. Deze aantrekkingskracht tussen moleculen noemen we de vanderwaalskracht.
De vanderwaalskracht is vernoemd naar de Nederlandse natuurkundige Johannes Diderik van der Waals, die hiervoor de Nobelprijs heeft ontvangen. Door deze aantrekkingskracht ontstaat er een verbinding tussen de moleculen. Deze verbinding heet de vanderwaalsbinding, ook wel de molecuulbinding genoemd. Het is belangrijk om te onthouden dat deze bindingen tussen moleculen bestaan, en niet binnen moleculen (dat zijn atoombindingen).
Invloed van molecuulmassa op de vanderwaalsbinding
Een belangrijke factor die de sterkte van de vanderwaalsbinding beïnvloedt, is de massa van de moleculen.
•Hoe groter de massa van een molecuul, hoe groter de vanderwaalskracht.
•Hoe groter de vanderwaalskracht, hoe sterker de vanderwaalsbinding.
Een sterkere vanderwaalsbinding betekent dat er meer energie nodig is om de moleculen van elkaar te scheiden. Dit heeft direct invloed op het kookpunt van een stof. Het kookpunt is de temperatuur waarbij een stof van de vloeistoffase overgaat naar de gasfase. Om dit te laten gebeuren, moeten de moleculen elkaar loslaten, wat betekent dat de vanderwaalsbindingen verbroken moeten worden.
•Hoe zwaarder een molecuul, hoe sterker de vanderwaalsbinding.
•Hoe sterker de vanderwaalsbinding, hoe meer warmte er nodig is om deze te verbreken.
•Hoe meer warmte er nodig is, hoe hoger het kookpunt.
Laten we dit bekijken aan de hand van een reeks koolwaterstoffen (alkanen):
Stof | Massa (in u) | Kookpunt (K) |
|---|---|---|
CH4 (g) | 16,04 | 112 |
C2H6 (g) | 30,07 | 185 |
C3H8 (g) | 44,09 | 231 |
C4H10 (g) | 58,12 | 273 |
C5H12 (l) | 72,15 | 309 |
C6H14 (l) | 86,17 | 342 |
Je ziet in de tabel duidelijk dat naarmate de molecuulmassa toeneemt, het kookpunt ook stijgt. De eerste vier stoffen (methaan t/m butaan) zijn bij kamertemperatuur (ongeveer 21 °C) gassen, omdat hun kookpunt lager is dan kamertemperatuur. Pentaan en hexaan zijn bij kamertemperatuur vloeistoffen, omdat hun kookpunt hoger is.
Invloed van molecuulvorm en contactoppervlak
Soms hebben moleculen dezelfde molecuulformule en dus dezelfde molecuulmassa, maar toch een verschillend kookpunt. Dit komt door de molecuulvorm en het contactoppervlak tussen de moleculen. Neem bijvoorbeeld butaan en methylpropaan. Beide hebben de molecuulformule C₄H₁₀ en een molecuulmassa van 58,12 U. Toch is het kookpunt van butaan (-0,5 °C) hoger dan dat van methylpropaan (-11,7 °C). Hoe kan dit?
Butaan versus methylpropaan
•Butaan heeft een onvertakte ketenstructuur. Je kunt het vergelijken met een langwerpig luciferpinnetje.
•Methylpropaan heeft een vertakte structuur, waardoor het molecuul ronder en compacter is. Dit lijkt meer op een bolletje.
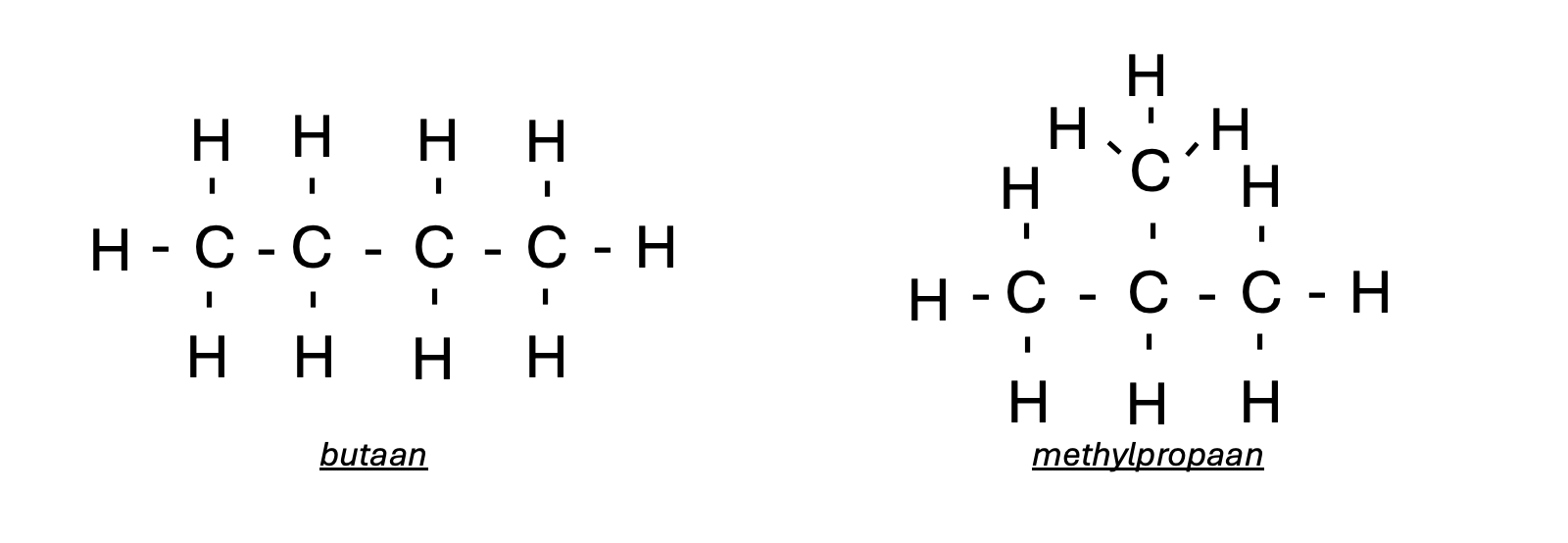
De vorm van het molecuul bepaalt hoe goed moleculen tegen elkaar aan kunnen liggen.
•Groter contactoppervlak: Langwerpige moleculen (zoals butaan) kunnen over een groter oppervlak contact maken met andere langwerpige moleculen. Ze kunnen dichter bij elkaar komen.
•Kleiner contactoppervlak: Bolvormige moleculen (zoals methylpropaan) hebben minder contactoppervlak met elkaar. Ze kunnen minder dicht bij elkaar komen.
Hoe dichter moleculen bij elkaar kunnen komen, hoe kleiner de afstand tussen hun massa's. En hoe kleiner de afstand, hoe groter de vanderwaalskracht en dus hoe sterker de vanderwaalsbinding.
•Butaan heeft een groter contactoppervlak, waardoor de vanderwaalsbindingen sterker zijn en het kookpunt hoger is.
•Methylpropaan heeft een kleiner contactoppervlak, waardoor de vanderwaalsbindingen zwakker zijn en het kookpunt lager is.
Waarom is hexaan een vloeistof en methaan een gas bij kamertemperatuur?
Nu kunnen we de centrale vraag beantwoorden: waarom is hexaan (C₆H₁₄) bij kamertemperatuur een vloeistof en methaan (CH₄) een gas?
1.Molecuulmassa: Hexaan (86,17 U) heeft een aanzienlijk grotere molecuulmassa dan methaan (16,04 U).
2.vanderwaalskracht en -binding: Door de grotere massa van hexaan zijn de vanderwaalskrachten tussen hexaanmoleculen sterker dan die tussen methaanmoleculen. Dit resulteert in sterkere vanderwaalsbindingen bij hexaan.
3.Kookpunt: Sterkere bindingen betekenen dat er meer energie nodig is om de moleculen van elkaar te scheiden. Het kookpunt van hexaan is 69 °C, terwijl het kookpunt van methaan -161 °C is.
4.Fase bij kamertemperatuur: Bij kamertemperatuur (ongeveer 21 °C) is de temperatuur ruim boven het kookpunt van methaan, waardoor het een gas is. De temperatuur is echter ruim onder het kookpunt van hexaan, waardoor het een vloeistof is.













