Nucleofiel deeltje
Vink alle eigenschappen aan die ertoe kunnen leiden dat een deeltje nucleofiel is.


Test je kennis met de 4 examenvragen die aan dit onderwerp zijn gekoppeld.
Vink alle eigenschappen aan die ertoe kunnen leiden dat een deeltje nucleofiel is.
In deze les leer je over nucleofiel en elektrofiele deeltjes in reactiemechanismen. Wat zijn de eigenschappen van deze deeltjes? En hoe herken je deze nucleofiel en elektrofiele deeltjes in een reactiemechanisme?
Een reactiemechanisme beschrijft het proces waarin atoombindingen worden verbroken en nieuwe worden gevormd. Het geeft ons een kijkje in welke volgorde deze gebeurtenissen plaatsvinden en hoe dit leidt tot het eindproduct van de reactie. Interessant zijn ook de tussenproducten die tijdens verschillende stappen verschijnen. Deze mechanismen maken vaak gebruik van Lewisstructuren om de interacties van bindende en niet-bindende elektronen te tonen.
Bindende en niet-bindende elektronen spelen een centrale rol in reactiemechanismen. Ze bepalen hoe en waar een reactie kan plaatsvinden, wat cruciaal is voor het begrijpen van de chemie achter de reacties.
In de fascinerende wereld van chemische reacties vormen nucleofielen en elektrofielen de essentiële elementen waaromheen veel reacties zijn georganiseerd. Laten we hun eigenschappen en werkingen nader onderzoeken.
Nucleofielen zijn deeltjes met een elektronenoverschot, wat inhoudt dat ze "kern-lievend" zijn. Ze zijn aangetrokken tot positief geladen delen van andere moleculen of ionen. Dit kunnen negatief geladen ionen zijn of moleculen met een niet-bindend elektronenpaar of dubbele bindingen. Voorbeelden hiervan zijn:
•Ammoniak (NH3) met een niet-bindend elektronenpaar op het stikstofatoom.
•Water (H₂O), waar het zuurstofatoom een niet-bindend elektronenpaar heeft.
•Etheen (C2H4) door zijn dubbele bindingen.
Elektrofielen, aan de andere kant, zijn deeltjes die "elektronen-lievend" zijn. Ze hebben een elektropositief lading of een positief geladen deel van een molecuul, vaak als gevolg van een polaire binding. Ze zoeken naar plaatsen waar ze elektronen kunnen ontvangen van nucleofielen. Voorbeelden zijn:
•Waterstofchloride (HCl), met een polaire binding die een delta plus en delta min oplevert.
•Carbokationen, positief geladen koolstofdeeltjes.
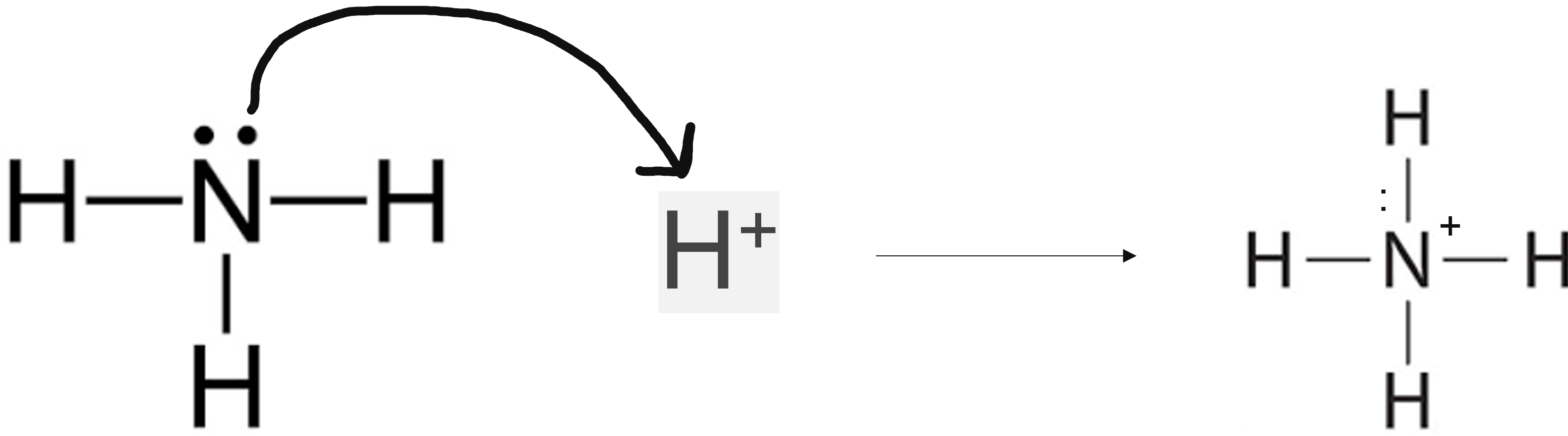
Bovenstaand diagram toont hoe een nucleofiel deeltje, zoals ammoniak, een elektrofiel deeltje, zoals H+, aantrekt en ermee reageert, wat resulteert in een nieuw molecuul.
Een uitgelichte reactiemechanisme in deze context is de additiereactie tussen etheen en waterstofchloride. Etheen, met een elektronenoverschot, functioneert hier als nucleofiel en valt het elektrofiele H-atoom van HCl aan. Dit leidt tot het breken en vormen van nieuwe bindingen, wat resulteert in de vorming van chloroethaan en een chloride-ion.
1.Etheen valt H van HCl aan, aangezien het een delta plus lading draagt.
2.Vorming van chloroethaan: Het glooratoom wordt een chloride-ion.
3.Reactieproducten: De uiteindelijke producten zijn chloroethaan en een chloride-ion.
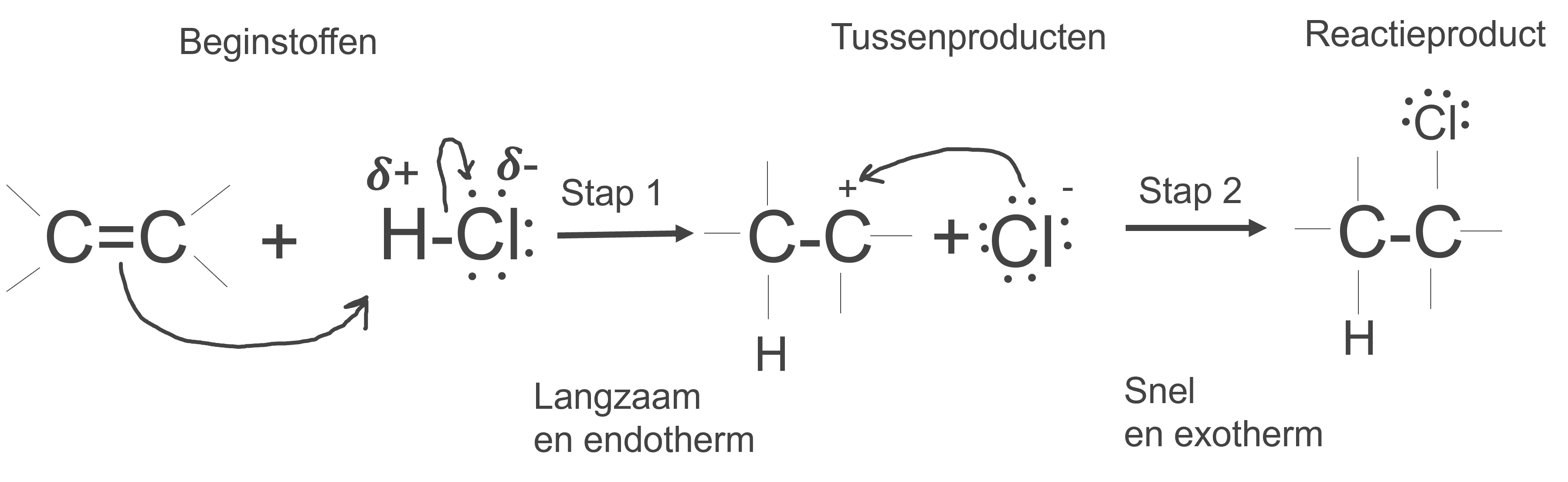
Dit reactiestaafdiagram laat de energieveranderingen zien in de eerste, endotherme, langzame stap en de snelle exotherme tweede stap, waarbij warmte vrijkomt.
Alle informatie die ik voor mijn toetsen moet kennen is aanwezig, de powerpoints zijn duidelijk en makkelijk te begrijpen. De opdrachten passen altijd goed bij het onderwerp en ondersteunen goed bij het leren. JoJoschool is erg overzichtelijk voor mij!
Ik gebruik het nu voor Biologie, het werkt ontzettend goed, het is heel overzichtelijk en alles wordt behandeld. Hoog rendement haal ik met leren, geen langdradige verhalen, maar ook niet te moeilijk. Het houdt ook automatisch bij hoe ver je bent.
Het is voor mij een erg goede manier om de leerstof voor toetsen te begrijpen. De video’s zijn een stuk duidelijker en beter dan de meeste video’s op YouTube.

86% van onze leerlingen zegt hoger te scoren.

Een alternatief op dure bijles, altijd uitgelegd door bevoegde docenten.

83% van onze leerlingen zegt onderwerpen sneller te begrijpen.







