Corrosie voorkomen
Op welke 3 manieren kan je corrosie van metalen voorkomen?


 Thijs Brouwer
Thijs BrouwerOp welke 3 manieren kan je corrosie van metalen voorkomen?
•Je kunt uitleggen wat de edelheid en corrosiegevoeligheid van metalen zijn.
•Je kunt micro- en mesostructuur en macro-eigenschappen van metalen uitleggen.
Edele metalen, zoals goud, zilver en platina, zijn niet erg reactief. Dit betekent dat ze niet makkelijk reageren met andere stoffen, zoals zuurstof uit de lucht. Hierdoor vind je deze metalen vaak in hun zuivere vorm in de grond. Andere metalen, zoals ijzer, koper en nikkel, zijn minder edel. Ze reageren wel makkelijk met zuurstof en komen daarom vaak voor als metaaloxide in de grond. Denk hierbij aan ijzererts, dat voornamelijk uit ijzeroxide bestaat. Feitelijk zijn deze metalen in de grond al verroest of gecorrodeerd.
Om van een metaaloxide weer zuiver metaal te maken, moet je het oxide laten reageren met een reductor. Een reductor is een stof die elektronen afstaat. De metaalionen in het oxide (bijvoorbeeld ijzerionen, koperionen of nikkelionen) nemen deze elektronen op en worden zo weer omgezet in zuiver metaal. Dit proces is eigenlijk het omgekeerde van roesten.
Stel je voor dat het Vrijheidsbeeld, dat van koper is gemaakt, zou veranderen in koperoxide. Koper reageert met zuurstof (de oxidator) en vormt koperoxide (2 Cu + O2 → 2 CuO). Hierbij ontstaan koper(II)ionen (Cu2+) en oxide-ionen (O2-). Om van dit koperoxide weer zuiver koper te maken, moeten we elektronen toevoegen aan de koper(II)ionen. Dit doen we door een sterkere reductor toe te voegen, die de elektronen levert. Zo draaien we het proces om en krijgen we weer zuiver koper.
Corrosie, oftewel het roesten van metalen, is een ongewenst proces in onze leefomgeving. We willen voorkomen dat metalen voorwerpen zoals bruggen, auto's of fietsen door roest worden aangetast. Er zijn verschillende manieren om corrosie tegen te gaan:
1.Afdekken met een verflaag: Dit is een veelgebruikte methode. Denk aan verkeersborden of de lak op je fiets. De verflaag vormt een fysieke barrière die voorkomt dat water en zuurstof in contact komen met het metaal, waardoor corrosie wordt tegengegaan.
2.Afdekken met een laagje ander metaal (verzinken): Bij deze methode wordt het te beschermen metaal bedekt met een laagje van een ander, vaak minder edel, metaal. Een bekend voorbeeld is verzinken, waarbij staal wordt bedekt met een laagje zink.
•Het te beschermen materiaal wordt in een bad met gesmolten zink gehangen.
•Na het omhooghalen en drogen, zit er een laagje zink op het materiaal.
•Dit zink reageert vervolgens met zuurstof uit de lucht tot zinkoxide.
•Het zinkoxide vormt een goed afsluitend laagje dat het onderliggende metaal beschermt tegen verdere corrosie.

3.Afdekken met olie: Bij onderdelen zoals een fietsketting wordt vaak olie gebruikt. Olie is hydrofoob, wat betekent dat het water afstoot. Door een laagje olie aan te brengen, wordt voorkomen dat water en zuurstof bij het metaal komen, waardoor roesten wordt vertraagd.
Om de eigenschappen van metalen goed te begrijpen, kijken we naar drie verschillende niveaus: micro, meso en macro. Niet alle eigenschappen zijn vanuit elk niveau te verklaren.
Op microniveau bekijken we de allerkleinste deeltjes: één positief geladen metaalion en één elektron. Dit niveau is te klein om met het blote oog te zien.
Het mesoniveau zit tussen micro en macro in. Hier bekijken we een klein stukje van het metaal, bestaande uit meerdere positief geladen metaalionen die gerangschikt zijn in een regelmatig patroon, het metaalrooster. Tussen deze metaalionen bewegen de vrije valentie-elektronen zich vrijelijk. Deze elektronen worden ook wel de 'elektronenzee' genoemd.
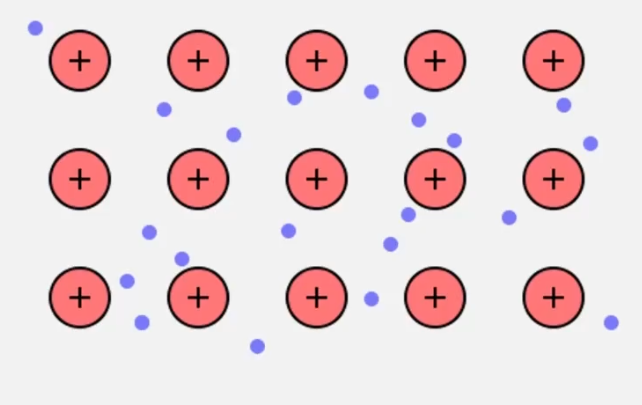
Vanuit het mesoniveau kunnen we belangrijke eigenschappen van metalen verklaren:
•Elektrische geleiding: Omdat de valentie-elektronen vrij kunnen bewegen door het hele metaalrooster, kunnen ze gemakkelijk elektrische stroom transporteren. Dit verklaart waarom metalen, zoals koper in elektriciteitskabels, goede elektrische geleiders zijn.
•Hoge smeltpunten: De metaalbinding tussen de positieve metaalionen en de vrije elektronen is erg sterk. Om deze binding te verbreken en het metaal te laten smelten, is veel energie nodig, wat resulteert in hoge smeltpunten. Denk aan ijzer dat je flink moet verhitten om het te smelten.
Het macroniveau is wat je met je ogen kunt zien en direct kunt waarnemen. Dit is bijvoorbeeld een blok metaal.
Op macroniveau kun je bijvoorbeeld de volgende eigenschappen waarnemen:
•Elektrische geleiding: Je kunt een blok metaal aansluiten op een batterij en een lampje. Als het lampje gaat branden, zie je op macroniveau dat het metaal geleidt.
•Buigzaamheid: Je kunt een stuk metaal vastpakken en buigen. De buigzaamheid is een eigenschap die je direct waarneemt op macroniveau.
Het is belangrijk om te onthouden dat je niet alle eigenschappen vanuit elk niveau kunt verklaren. De vrije elektronen die de geleiding verklaren, zijn bijvoorbeeld alleen goed te visualiseren op mesoniveau, niet op microniveau met slechts één ion en één elektron.
Zuivere metalen zijn vaak relatief zacht. Dit komt doordat de lagen van positief geladen metaalionen in het metaalrooster gemakkelijk over elkaar heen kunnen schuiven, terwijl de vrije elektronen de boel bij elkaar houden.

Dit is een belangrijk verschil met zouten, die geen vrije elektronen hebben en daardoor bij belasting vaak breken in plaats van buigen.
Om metalen harder en sterker te maken, worden vaak legeringen gemaakt. Een legering is een mengsel van twee of meer metalen, of een metaal met een niet-metaal. Een bekend voorbeeld is brons, een legering van koper en tin.
Hoe maakt een legering een metaal harder? Door een ander atoom (dat kleiner of groter is dan de atomen van het hoofdmetaal) in het metaalrooster te brengen, ontstaat een roosterfout of verstoring. Deze verstoring zorgt ervoor dat de lagen van metaalionen niet meer zo gemakkelijk over elkaar heen kunnen schuiven.
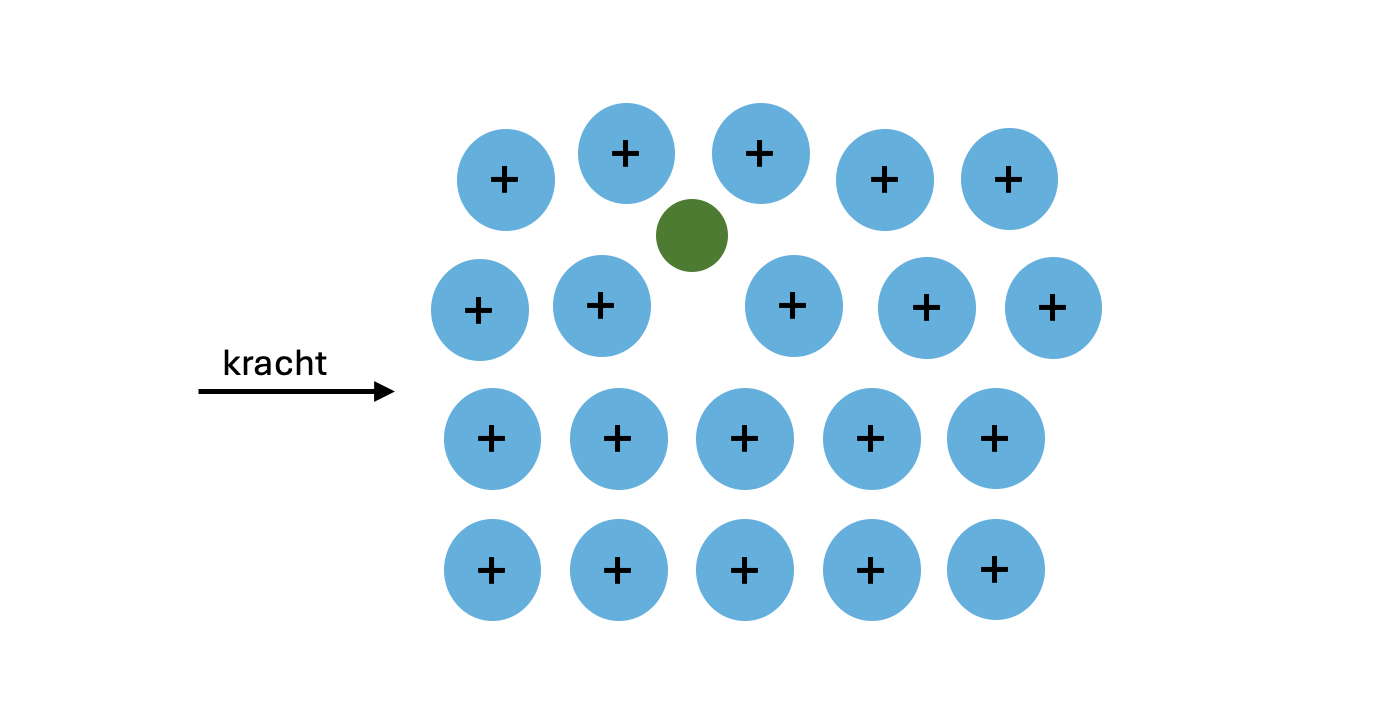
Wanneer je nu druk uitoefent op het materiaal, worden de lagen tegengehouden door de ingebrachte atomen. Hierdoor wordt het materiaal harder en minder buigzaam dan het zuivere metaal. Elke verstoring in het rooster, of het nu door een kleiner of groter atoom komt, leidt ertoe dat de lagen moeilijker te verschuiven zijn, waardoor de legering uiteindelijk harder wordt.
Een fascinerende legering is Nitinol. Dit is een voorbeeld van een geheugenmateriaal. Het heeft de bijzondere eigenschap dat het na vervorming terugkeert naar zijn oorspronkelijke vorm wanneer het wordt verwarmd.
Stel je voor dat je een staaf van Nitinol hebt.
1.Je verwarmt deze staaf tot ongeveer 500 graden Celsius en brengt hem in een specifieke, gewenste vorm (bijvoorbeeld een perfect rechte staaf).
2.Vervolgens koel je de staaf af.
3.Na afkoeling kun je de staaf in een andere vorm buigen, bijvoorbeeld een kromme vorm die past bij een ruggengraat die rechtgezet moet worden.
4.Wanneer deze verbogen Nitinol staaf vervolgens wordt blootgesteld aan een hogere temperatuur, zoals de lichaamstemperatuur van 37 graden Celsius (kamertemperatuur is ongeveer 25 graden Celsius), gebeurt er iets bijzonders. Door de warmte 'herinnert' het materiaal zich de vorm die het had bij 500 graden Celsius.
5.De staaf zal dan vanzelf terugkeren naar zijn oorspronkelijke rechte vorm.

Dit fenomeen wordt verklaard doordat Nitinol tussen twee verschillende roosterstructuren kan wisselen, afhankelijk van de temperatuur. Bij een hogere temperatuur neemt het de ene structuur aan, en bij een lagere temperatuur een andere. Door het materiaal bij een hoge temperatuur in een bepaalde vorm te 'trainen', slaat het die vorm op als zijn 'geheugen'. Wanneer het later weer tot die temperatuur wordt verwarmd, keert het terug naar die opgeslagen vorm. Deze eigenschap maakt Nitinol zeer waardevol voor toepassingen in bijvoorbeeld de medische wereld, zoals het rechtzetten van ruggenwervels.
Alle informatie die ik voor mijn toetsen moet kennen is aanwezig, de powerpoints zijn duidelijk en makkelijk te begrijpen. De opdrachten passen altijd goed bij het onderwerp en ondersteunen goed bij het leren. JoJoschool is erg overzichtelijk voor mij!
Ik gebruik het nu voor Biologie, het werkt ontzettend goed, het is heel overzichtelijk en alles wordt behandeld. Hoog rendement haal ik met leren, geen langdradige verhalen, maar ook niet te moeilijk. Het houdt ook automatisch bij hoe ver je bent.
Het is voor mij een erg goede manier om de leerstof voor toetsen te begrijpen. De video’s zijn een stuk duidelijker en beter dan de meeste video’s op YouTube.

86% van onze leerlingen zegt hoger te scoren.

Een alternatief op dure bijles, altijd uitgelegd door bevoegde docenten.

83% van onze leerlingen zegt onderwerpen sneller te begrijpen.







