Leg uit wat een index in een molecuulformule betekent en geef een voorbeeld.
Leerdoelen
•Je kunt de molecuulformule van een stof afleiden uit de structuurformule
•Je kunt de molecuulformules van de acht twee-atomige elementen geven
•Je kunt de molecuulformules geven van acht verbindingen
•Je kunt het massapercentage van een atoomsoort in een verbinding berekenen
Molecuulformules
In de scheikunde wordt de molecuulformule gebruikt om de samenstelling van een verbinding weer te geven. Deze formule bevat het symbool van elk atoom en een index die aangeeft hoeveel van dat atoom aanwezig is. Bijvoorbeeld de molecuulformule van water is H2O wat betekent dat er twee waterstofatomen en één zuurstofatoom in elk watermolecuul zitten.
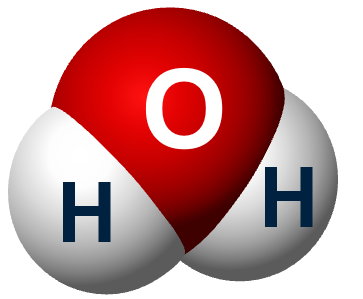
Het afleiden van molecuulformules
Je leert de molecuulformule afleiden uit een structuurformule of uit een molecuultekening. Voorbeelden van molecuultekeningen zijn:
•Water: (H₂O) - twee waterstofatomen en één zuurstofatoom.
•Koolstofdioxide: (CO��₂) - één koolstofatoom en twee zuurstofatomen.
•Glucose: (C6H12O6) - zes koolstofatomen, twaalf waterstofatomen en zes zuurstofatomen.
Groepen van atomen
Soms worden groepen van atomen in een molecuul apart weergegeven. Dit geeft extra informatie over de structuur.
Voorbeeld: azijnzuur
De formule van azijnzuur is (CH3COOH). Hieruit blijkt dat het molecuul zowel een (CH3) deel als een (COOH) zuurgroep bevat, wat belangrijk is voor de chemische eigenschappen van azijnzuur.
.
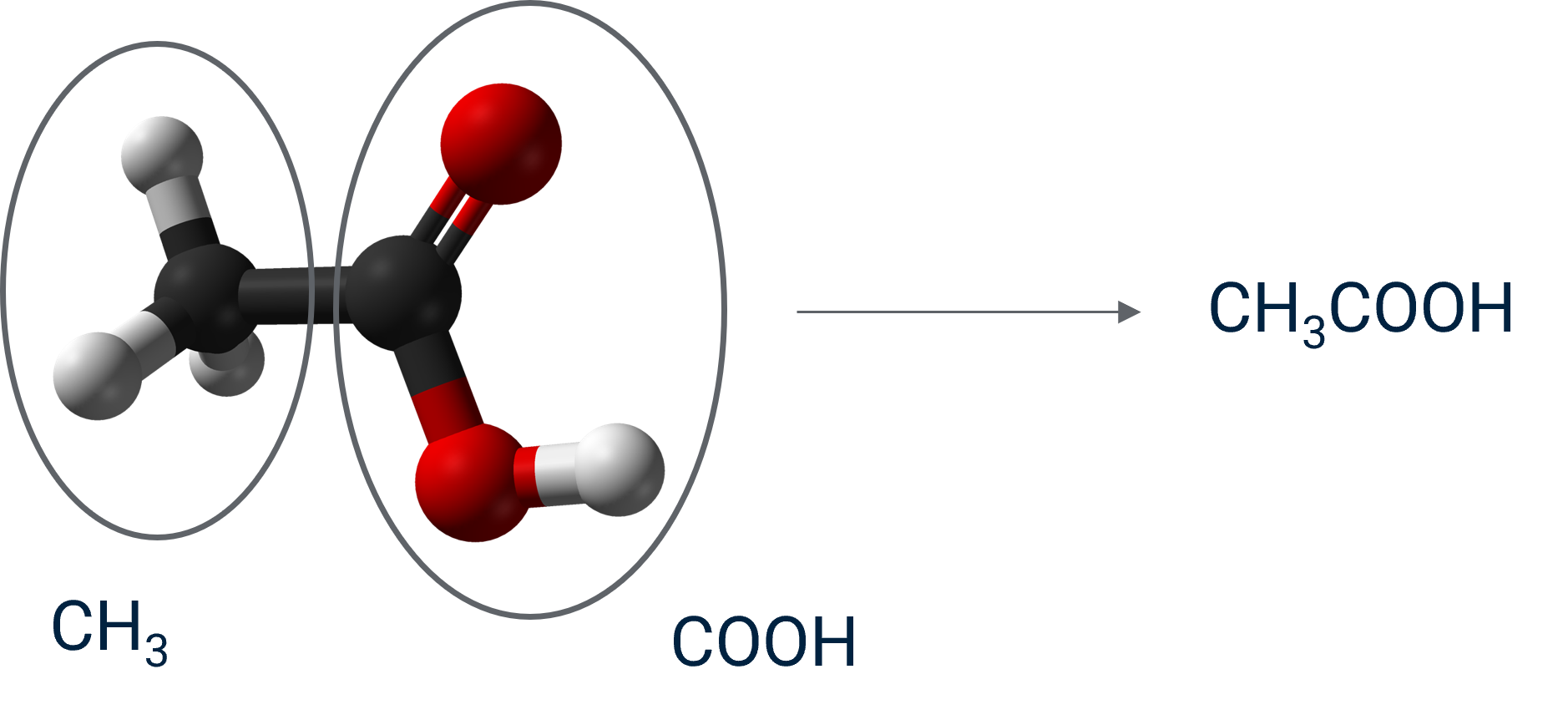
Coëfficiënten en index
De coëfficiënt in een molecuulformule geeft aan hoeveel moleculen van een bepaalde verbinding aanwezig zijn. Bijvoorbeeld in de formule (7 CH3COOH) betekent de 7 dat er 7 van dat molecuul aanwezig zijn.
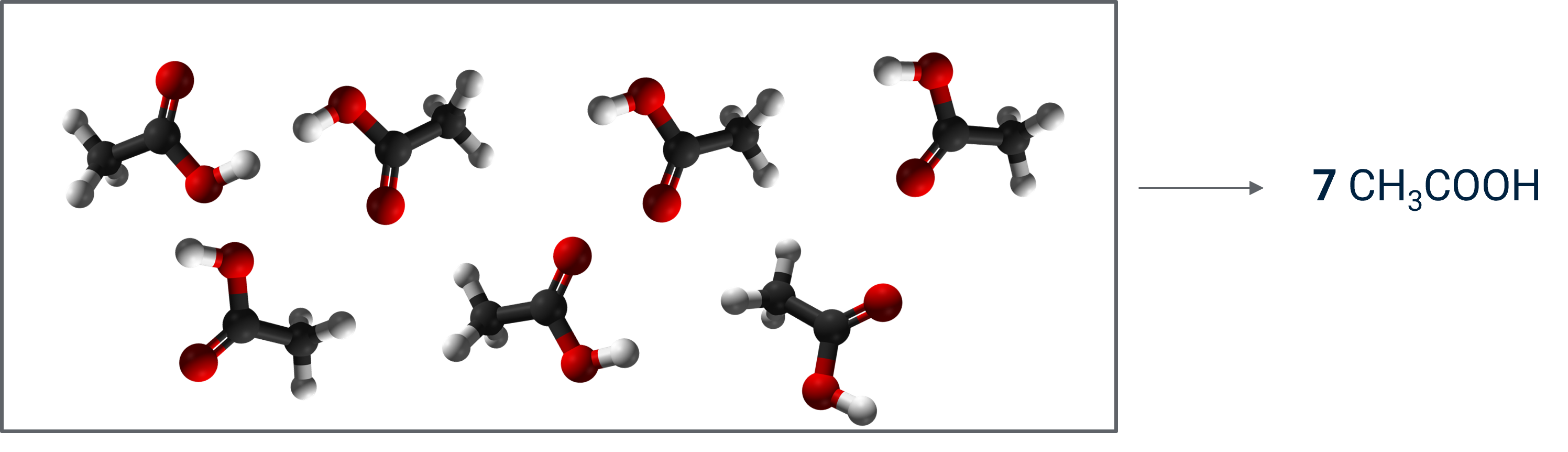
Belangrijke molecuulformules
Er zijn een aantal molecuulformules die je vaak tegen gaat komen en is dus handig om uit je hoofd te kennen.
Dat zijn de volgende moleculen:
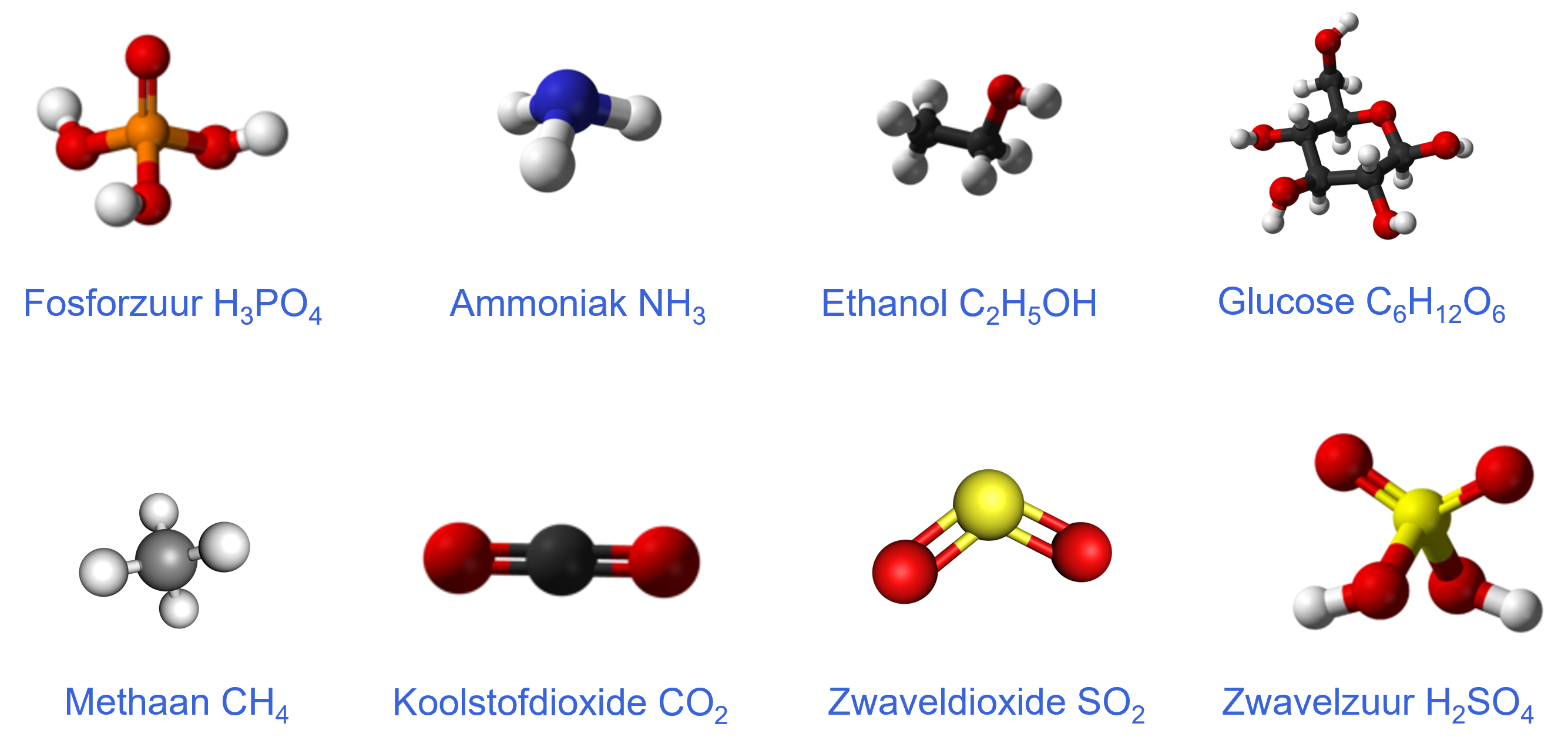
Twee-atomige elementen
In de natuur zijn er zeven twee-atomige elementen die altijd in paren voorkomen als ze als gas of enkelvoudige stof voorkomen. Deze elementen zijn:
•Chloor (Cl2)
•Fluor (F2)
•Stikstof (N2)
•Waterstof (H2)
•Zuurstof (O2)
•Jood (I2)
•Broom (Br2)
Om deze te onthouden kun je de ezelsbrug als volgt gebruiken: "Claire Fietst Naar Haar Oma In Brussel". Elke beginletter komt overeen met een van de twee-atomige elementen.
Atoommassa
Elke atoommassa wordt uitgedrukt in atomaire massa-eenheden (u). Één (u) is gelijk aan 1{,}66\cdot10^{-27}1{,}66\cdot10^{-2}1{,}66\cdot10^{-}1{,}66\cdot101{,}66\cdot11{,}66\cdot1{,}661{,}61{,}1kg. Enkele voorbeelden zijn:
•Waterstof (H): 1 u
•Koolstof (C): 12 u
•Stikstof (N): 14 u
•Zuurstof (O): 16 u
Bijvoorbeeld de massa van glucose (C6H12O6) kan worden berekend door het optellen van de atoommassa's:
Dan volgt:
6\cdot12+12\cdot1+6\cdot16=180u6\cdot12+12\cdot1+6\cdot16=1806\cdot12+12\cdot1+6\cdot16=186\cdot12+12\cdot1+6\cdot16=16\cdot12+12\cdot1+6\cdot16=6\cdot12+12\cdot1+6\cdot166\cdot12+12\cdot1+6\cdot16\cdot12+12\cdot1+6\cdot6\cdot12+12\cdot1+66\cdot12+12\cdot1+6\cdot12+12\cdot1+16\cdot12+12\cdot1+126\cdot12+12\cdot1+16\cdot12+12\cdot1+6\cdot12+12\cdot16\cdot12+12\cdot6\cdot12+126\cdot12+16\cdot12+6\cdot126\cdot16\cdot6
De atomaire massa van glucose is dus gelijk aan 180 u (let op in dit voorbeeld zijn een aantal waardes naar hele getallen afgerond).













