Wanneer waterstof en zuurstof met elkaar reageren ontstaat er 10 g water. Dit is een exotherme reactie.
Bezitten de beginstoffen (waterstof en zuurstof) of het reactieproduct water de meeste chemische energie?


 Thijs Brouwer
Thijs BrouwerTest je kennis met de 9 examenvragen die aan dit onderwerp zijn gekoppeld.
Wanneer waterstof en zuurstof met elkaar reageren ontstaat er 10 g water. Dit is een exotherme reactie.
Bezitten de beginstoffen (waterstof en zuurstof) of het reactieproduct water de meeste chemische energie?
•Je kunt de kenmerken van een chemische reactie uitleggen
•Je kunt uitleggen welke mogelijke energie-effecten er zijn
•Je kunt uitleggen hoe een energiediagram eruitziet
Elke chemische reactie start met beginstoffen en resulteert in reactieproducten. De beginstoffen staan voor de pijl en de reactieproducten na de pijl. Een andere naam voor beginstoffen is 'reactanten' en een andere naam voor reactieproducten is 'producten'.
De totale massa van de beginstoffen is gelijk aan de massa van de reactieproducten, wat bekend staat als de wet van behoud van massa, of de wet van Lavoisier.
Bijvoorbeeld bij de reactie2\text{Cu} + \text{O}_2 + 2\text{CO}_2 \rightarrow 2\text{CuCO}_32\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2\operatorname{CuCO_3}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2\operatorname{cCuCO_3}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2\operatorname{cCuCO_3m}}2\operatorname{Cu+}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2\operatorname{cCuCO_3}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2\operatorname{cCuCO_3m}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2\operatorname{cCuCO_3}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2\operatorname{cCuCO_3m}}2\operatorname{Cu+}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2\operatorname{cCuCO_3m}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2\operatorname{cCuC_3m}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2\operatorname{cCuCo_3m}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2\operatorname{cCuCom}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2\operatorname{cCuCm}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2\operatorname{cCum}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2\operatorname{cCm}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2\operatorname{cm}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2c}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow2}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}\rightarrow}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}\rightarrow}2\operatorname{Cu+}\operatorname{O_2+2\rightarrow}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}\rightarrow}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2\longrightarrow{}}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2--}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2-}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2-}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2--}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2--?}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2--}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2-}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{CO_2}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{cCO_2}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{cCO_2m}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{cCOm}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{cCm}}2\operatorname{Cu+}\operatorname{O_2+2\operatorname{cm}}2\operatorname{Cu+}\operatorname{O_2+2c}2\operatorname{Cu+}\operatorname{O_2+2}2\operatorname{Cu+}\operatorname{O_2+2C}2\operatorname{Cu+}\operatorname{O_2+2}2\operatorname{Cu+}\operatorname{O_2+}2\operatorname{Cu+}\operatorname{O_2}2\operatorname{Cu+}\operatorname{O_2m}2\operatorname{Cu+}\operatorname{cO_2m}2\operatorname{Cu+}\operatorname{cOm}2\operatorname{Cu+}\operatorname{cm}2\operatorname{Cu+}c2\operatorname{Cu+}2\operatorname{Cu+}O2\operatorname{Cu+}2\operatorname{cCu+}2\operatorname{cCum+}2\operatorname{cCum}2\operatorname{cCm}2\operatorname{cm}2c22\text{C}2\text{Cu}22222222222C2Cu2C2, is de massa aan de linkerkant gelijk aan2\cdot63{,}5+32{,}0+2\cdot44{,}0=247\text{ u}2\cdot63{,}5+32{,}0+2\cdot44{,}0=2472\cdot63{,}5+32{,}0+2\cdot44{,}0=242\cdot63{,}5+32{,}0+2\cdot44{,}0=2462\cdot63{,}5+32{,}0+2\cdot44{,}0=242\cdot63{,}5+32{,}0+2\cdot44{,}0=22\cdot63{,}5+32{,}0+2\cdot44{,}0=2\cdot63{,}5+32{,}0+2\cdot44{,}02\cdot63{,}5+32{,}0+2\cdot44{,}2\cdot63{,}5+32{,}0+2\cdot442\cdot63{,}5+32{,}0+2\cdot42\cdot63{,}5+32{,}0+2\cdot2\cdot63{,}5+32{,}0+22\cdot63{,}5+32{,}0+2\cdot63{,}5+32{,}02\cdot63{,}5+32{,}2\cdot63{,}5+322\cdot63{,}5+32\cdot63{,}5+2\cdot63{,}52\cdot63{,}2\cdot632\cdot62\cdot2. De massa aan de rechterkant is gelijk aan2\cdot123{,}5=247\text{ u}2\cdot123{,}5=2472\cdot123{,}5=2472\cdot123{,}5=2472\cdot123{,}5=2472\cdot123{,}5=2472\cdot123{,}5=2472\cdot123{,}5=2472\cdot123{,}5=2472\cdot123{,}5=2472\cdot123{,}5=2472\cdot123{,}5=247\operatorname{cm}2\cdot123{,}5=247c2\cdot123{,}5=2472\cdot123{,}5=242\cdot123{,}5=2462\cdot123{,}5=24672\cdot123{,}5=2462\cdot123{,}5=242\cdot123{,}5=22\cdot123{,}5=2\cdot123{,}52\cdot123{,}2\cdot1232\cdot122\cdot12\cdot2. Deze atoommassa's kun je opzoeken in de Binas.
Reacties vinden plaats in vaste verhoudingen, aangeduid door de coëfficiënten in reactievergelijkingen. Dit zijn de getallen die vóór de stoffen staan, niet te verwarren met de kleine getalletjes rechtsonder de atoomsymbolen, die de index worden genoemd. Tijdens een chemische reactie worden de atomen van de beginstoffen opnieuw gerangschikt. Bijvoorbeeld bij2\text{CuCO}_3isde coëfficiënt ende index.
Om een chemische reactie te starten is een minimale reactietemperatuur vereist. Zonder deze minimale temperatuur vindt er geen reactie plaats.
Elke chemische reactie gaat gepaard met een energie-effect. Dit kan exotherm zijn, waarbij energie vrijkomt, of endotherm, waarbij energie geabsorbeerd wordt.
Een voorbeeld van een chemische reactie is de verandering van kleur van het Vrijheidsbeeld. Oorspronkelijk was het een glimmende koperkleur, maar door de jaren heen heeft het een groene tint ontwikkeld. Dat komt doordat koper reageert met zuurstof en koolstofdioxide uit de lucht, waardoor kopercarbonaat wordt gevormd. Dit is de reactie2\text{Cu}+\text{O}_2+2\text{CO}_2\rightarrow2\text{CuCO}_3. De kleurverandering duidt op een verandering van een stofeigenschap, wat kenmerkend is voor een chemische reactie.
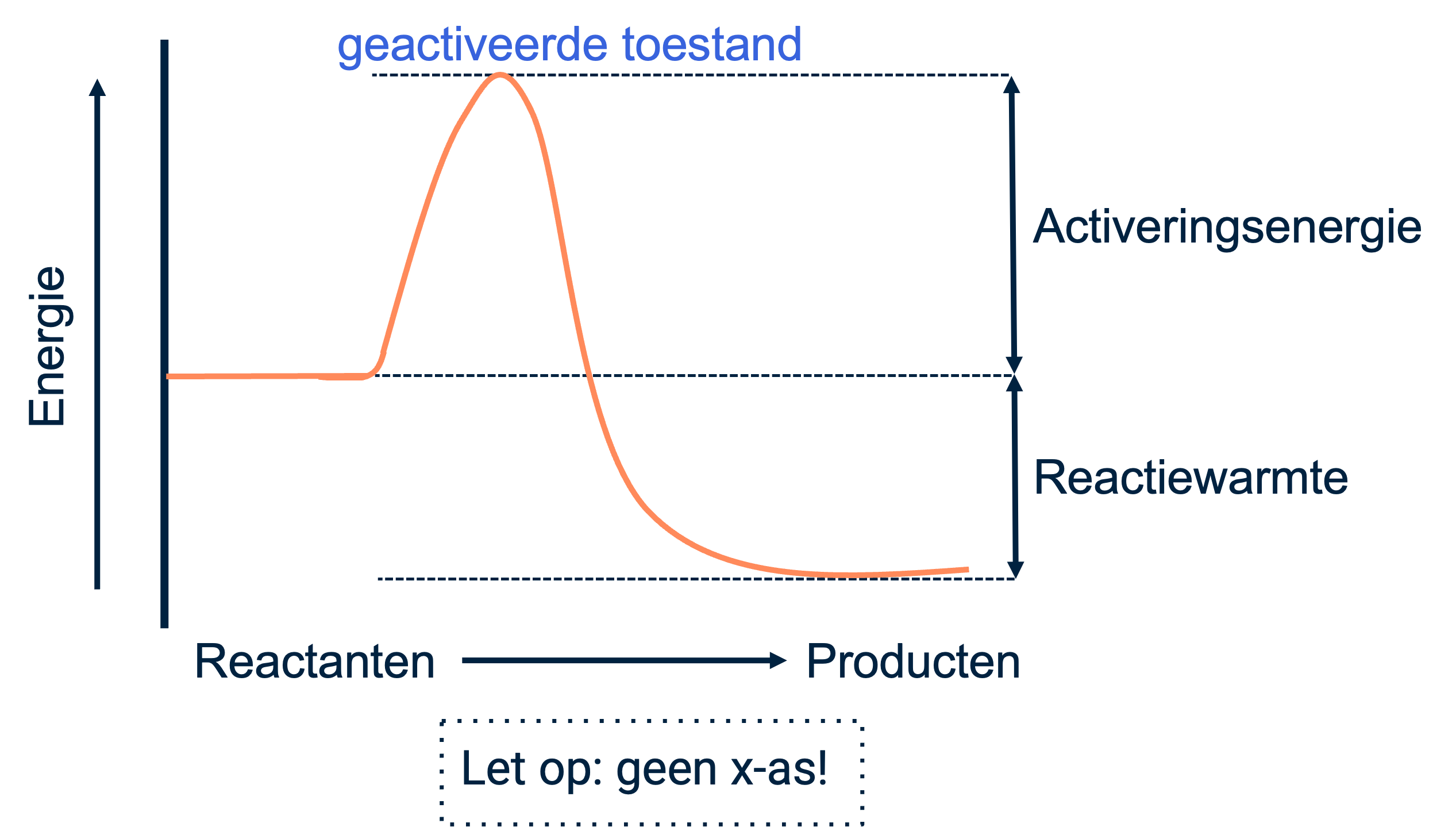
Een energiediagram toont de energieverandering tijdens een reactie. Het illustreert niet alleen de activeringsenergie die nodig is om de reactie te starten en naar de geactiveerde toestand te brengen, maar ook het verschil in energie tussen de beginstoffen en de reactieproducten. Deze energiewaarde heet de reactie-energie (of reactiewarmte,\Delta E\Delta).
Let op: een energiediagram heeft geen x-as, omdat het verloop van de reactie niet direct aan tijd gekoppeld is.
Bij exotherme reacties ligt het energieniveau van de reactieproducten (producten) lager dan dat van de beginstoffen (reactanten), wat betekent dat de reactie energie vrijgeeft, meestal in de vorm van warmte. Een kampvuur is een goed voorbeeld van een exotherme reactie. De verbranding van hout geeft energie vrij in de vorm van warmte en licht, wat je duidelijk kunt voelen en zien.
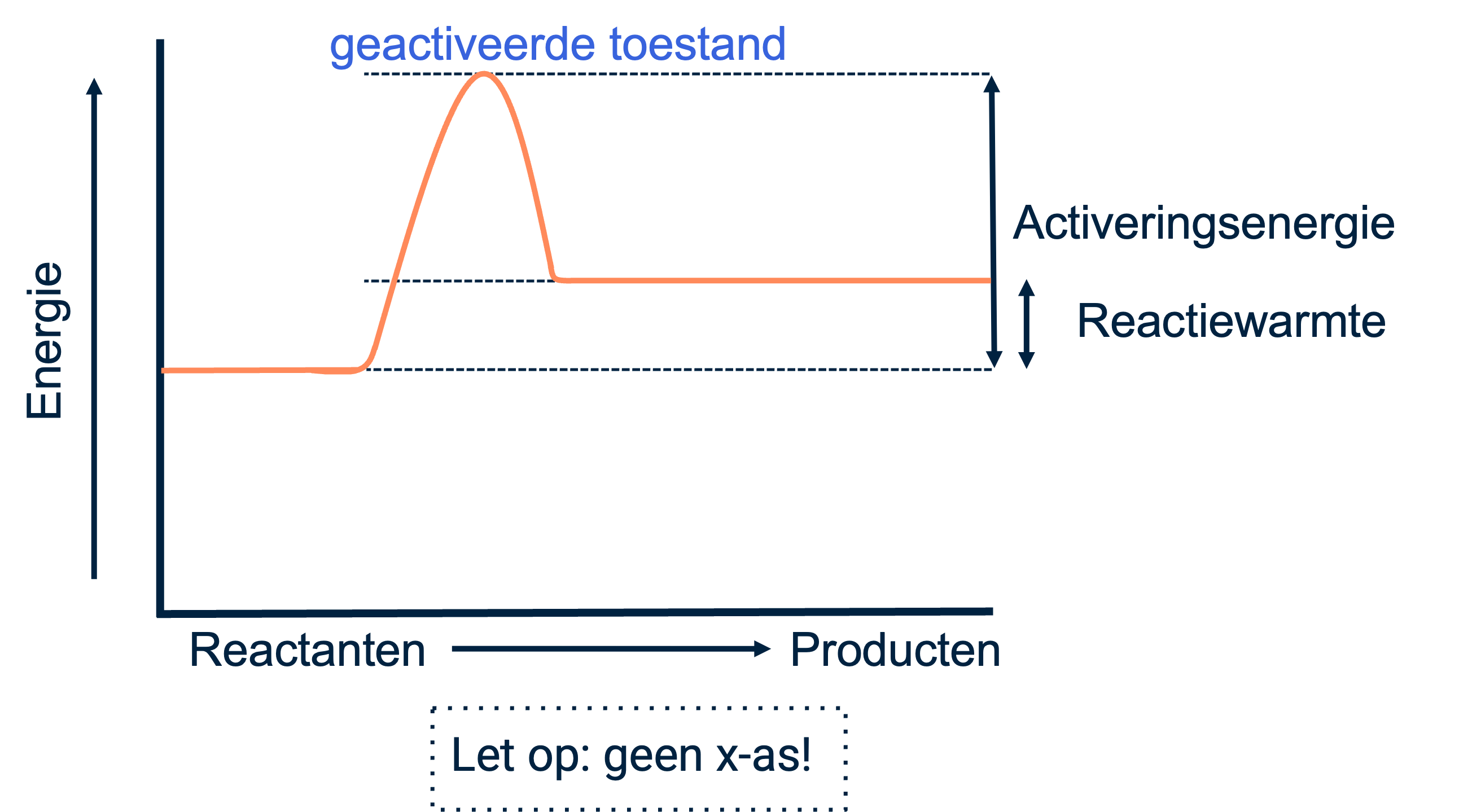
In tegenstelling tot exotherme reacties, vereisen endotherme reacties energie uit de omgeving om plaats te vinden. Het diagram toont een hoger energieniveau voor de reactieproducten vergeleken met de beginstoffen. Endotherme reacties hebben ook een activeringsenergie en een geactiveerde toestand.
Alle informatie die ik voor mijn toetsen moet kennen is aanwezig, de powerpoints zijn duidelijk en makkelijk te begrijpen. De opdrachten passen altijd goed bij het onderwerp en ondersteunen goed bij het leren. JoJoschool is erg overzichtelijk voor mij!
Ik gebruik het nu voor Biologie, het werkt ontzettend goed, het is heel overzichtelijk en alles wordt behandeld. Hoog rendement haal ik met leren, geen langdradige verhalen, maar ook niet te moeilijk. Het houdt ook automatisch bij hoe ver je bent.
Het is voor mij een erg goede manier om de leerstof voor toetsen te begrijpen. De video’s zijn een stuk duidelijker en beter dan de meeste video’s op YouTube.

86% van onze leerlingen zegt hoger te scoren.

Een alternatief op dure bijles, altijd uitgelegd door bevoegde docenten.

83% van onze leerlingen zegt onderwerpen sneller te begrijpen.







