Stel de halfreactie op voor de omzetting van ethanolC_2H_5OHC_2H_5OC_2H_5C_2HC_2C_2JC_2JHC_2JC_2C_{2H}C_2Cnaar acetaaldehydeCH_3CHOCH_3CHCH_3CCH_3CHCin zuur milieu. Zorg ervoor dat je rekening houdt met de massabalans en de ladingbalans.
Leerdoelen
•Je kunt primaire, secundaire en tertiaire alcoholen herkennen aan de structuurformule.
•Je kunt uitleggen dat alcoholen elektronen kunnen afstaan en dus als reductor kunnen optreden.
•Je kunt uitleggen hoe aldehyden als reductor elektronen afstaan.
Alcoholen als reductor
Alcoholen kunnen in chemische reacties optreden als reductor. Dit betekent dat ze elektronen afstaan aan een andere stof.
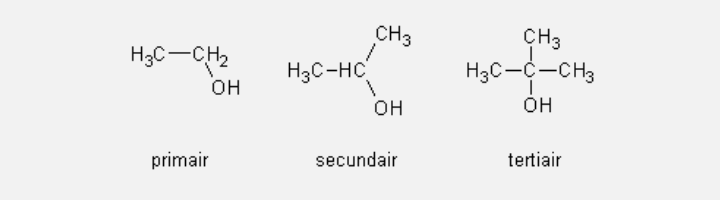
Primaire, secundaire en tertiaire alcoholen
Alcoholen worden ingedeeld in primair, secundair en tertiair, afhankelijk van het aantal koolstofatomen (C-atomen) dat gebonden is aan het koolstofatoom dat de OH-groep draagt.
Primair alcohol: het koolstofatoom met de OH-groep is gebonden aan één ander koolstofatoom.
Secundair alcohol: het koolstofatoom met de OH-groep is gebonden aan twee andere koolstofatomen.
Tertiair alcohol: het koolstofatoom met de OH-groep is gebonden aan drie andere koolstofatomen.
Oxidatie van alcoholen
Wanneer een alcohol als reductor optreedt, wordt deze geoxideerd. Dit betekent dat de OH-groep wordt omgezet in een carbonylgroep (C=O). Het type carbonylgroep dat gevormd wordt, hangt af van het type alcohol:
•Een primaire alcohol kan worden geoxideerd tot een aldehyde. Een aldehyde heeft een carbonylgroep aan het einde van de keten.
•Een secundaire alcohol kan worden geoxideerd tot een keton. Een keton heeft een carbonylgroep ergens in het midden van de keten.
•Een tertiaire alcohol kan niet direct worden geoxideerd. Dit komt doordat het koolstofatoom met de OH-groep al aan drie andere koolstofatomen gebonden is. Er is geen ruimte voor een dubbele binding met zuurstof zonder dat het koolstofatoom vijf bindingen aangaat, wat niet mogelijk is.
Halfreacties
De oxidatie van alcoholen kan worden weergegeven met behulp van halfreacties Hierbij wordt gekeken naar de uitwisseling van elektronen en protonen (H⁺), nooit met H₂.
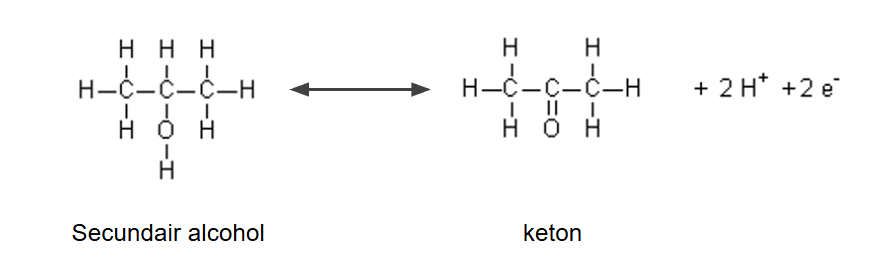
Voorbeeld 1: Propaan-2-ol als reductor
Propaan-2-ol is een secundaire alcohol en wordt geoxideerd tot een keton (propanon). De halfreactie is als volgt:
propaan-2-ol ⇌ propanon + 2 H⁺ + 2 e⁻
In deze reactie staat propaan-2-ol twee elektronen af (het is een reductor) en worden twee protonen gevormd. De reactie is in evenwicht, vandaar de dubbele pijl.
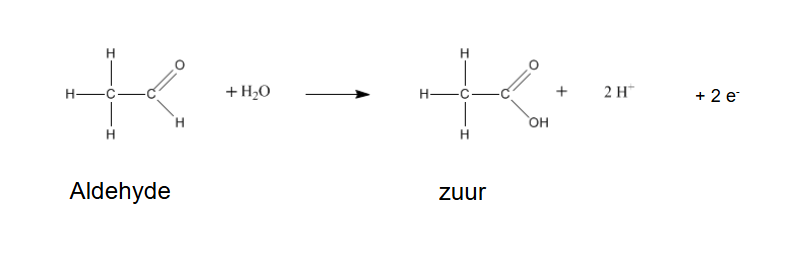
Voorbeeld 2: Een aldehyde als reductor
Een aldehyde kan verder worden geoxideerd tot een carboxylzuur. Hierbij wordt een zuurstofatoom toegevoegd aan de aldehydegroep (CHO), waardoor een carboxylgroep (COOH) ontstaat. De halfreactie is als volgt:
aldehyde + H₂O ⇌ carboxylzuur + 2 H⁺ + 2 e⁻
In deze reactie is water (H₂O) nodig om het extra zuurstofatoom te leveren. Er komen ook twee protonen en twee elektronen vrij.