Teken een stukje polypropeen waarin je twee monomeereenheden hebt verwerkt.



 Thijs Brouwer
Thijs BrouwerTeken een stukje polypropeen waarin je twee monomeereenheden hebt verwerkt.

•Je kunt uitleggen wat polymeren en monomeren zijn;
•Je kunt het verschil beschrijven tussen additiepolymerisatie en condensatiepolymerisatie;
•Je kunt de stappen initiatie, propagatie en terminatie benoemen en uitleggen;
•Je kunt herkennen of een polymeer via additiepolymerisatie is gevormd;
•Je kunt de structuurformule van een additiepolymeer opstellen uit het monomeer;
•Je kunt de repeterende eenheid van een polymeer aangeven en noteren.
Een polymeer is een groot molecuul dat bestaat uit een lange keten van kleine, herhalende bouwstenen. Deze bouwstenen worden monomeren genoemd. Het proces waarbij monomeren aan elkaar worden gekoppeld tot een polymeer heet polymerisatie.
Er bestaan twee soorten polymerisatie:
•Additiepolymerisatie
•Condensatiepolymerisatie
Bij additiepolymerisatie reageren monomeren met een dubbele binding tussen koolstofatomen (C=C) met elkaar. Deze dubbele binding klapt open, waardoor de monomeren aan elkaar kunnen koppelen. Een belangrijk kenmerk is dat de hoofdketen van het polymeer alleen uit koolstofatomen bestaat.
Bij condensatiepolymerisatie ontstaat het polymeer door een condensatiereactie waarbij een klein molecuul, meestal water, wordt afgesplitst. Hierbij spelen groepen zoals alcoholgroepen, zuurgroepen en aminogroepen een rol. Deze vorm wordt verder behandeld in een volgende les/video.
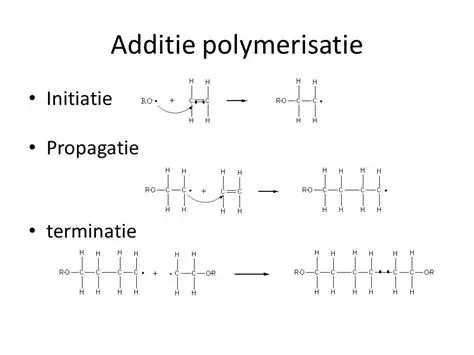
Additiepolymerisatie verloopt in drie stappen:
De reactie start met een initiator, vaak een peroxide. Wanneer de initiator wordt blootgesteld aan UV-straling, breekt de binding tussen twee zuurstofatomen. Daarbij ontstaan twee deeltjes met een vrij elektron. Deze zeer reactieve deeltjes heten radicalen.
Een radicaal wil graag een extra elektron krijgen om een binding te vormen, en is daarom erg reactief.
Tijdens de propagatie reageert het radicaal met een monomeer, bijvoorbeeld etheen. De dubbele binding van etheen klapt open en er ontstaat een nieuwe atoombinding tussen het radicaal en het monomeer. Het vrije elektron schuift door naar het uiteinde van de keten.
Dit proces herhaalt zich steeds opnieuw: er worden telkens nieuwe monomeren toegevoegd en de polymeerketen groeit.
Het aantal toegevoegde monomeren wordt aangeduid met n, wat vaak een groot getal is (bijvoorbeeld 10.000). Dit getal is een gemiddelde polymerisatiegraad.
De polymerisatie stopt bij de terminatie. Dit gebeurt wanneer twee radicalen elkaar ontmoeten en samen een nieuwe binding vormen. Het vrije elektron verdwijnt en de keten is niet langer reactief.
Terminatie kan plaatsvinden:
•tussen twee losse radicalen;
•of tussen twee groeiende polymeerketens.
Om de structuurformule van een additiepolymeer op te stellen, begin je bij het monomeer. De dubbele binding verdwijnt en wordt vervangen door enkelvoudige bindingen tussen de monomeren.
Voorbeeld:
•monomeer: etheen
•polymeer: polyetheen
De naam van het polymeer is altijd: poly + naam van het monomeer
De repeterende eenheid is het deel van het molecuul dat zich steeds herhaalt. Bij polyetheen is dat:
Omdat polymeren erg lang zijn, gebruiken we een verkorte weergave:
•repeterende eenheid tussen blokhaken
•met een subscript n
Een andere manier is het tekenen van een stukje uit het midden van de keten met tildes (~) aan beide uiteinden. Dit geeft aan dat de keten daar verder loopt.
Additiepolymeren zoals polyvinylchloride (PVC) en polyetheen worden op grote schaal gebruikt in de industrie. PVC wordt onder andere gebruikt voor het maken van regenpijpen en andere bouwmaterialen, dankzij zijn duurzaamheid en weerbestendigheid. Polyetheen is te vinden in een breed scala van producten, van verpakkingsmaterialen tot isolaties.
Polymeer | Monomeer | Toepassingen |
|---|---|---|
Polyetheen | Etheen | Verpakkingen, plastic tassen, flessen |
Polyvinylchloride (PVC) | Vinylchloride | Buizen, ramen, creditcards |
Alle informatie die ik voor mijn toetsen moet kennen is aanwezig, de powerpoints zijn duidelijk en makkelijk te begrijpen. De opdrachten passen altijd goed bij het onderwerp en ondersteunen goed bij het leren. JoJoschool is erg overzichtelijk voor mij!
Ik gebruik het nu voor Biologie, het werkt ontzettend goed, het is heel overzichtelijk en alles wordt behandeld. Hoog rendement haal ik met leren, geen langdradige verhalen, maar ook niet te moeilijk. Het houdt ook automatisch bij hoe ver je bent.
Het is voor mij een erg goede manier om de leerstof voor toetsen te begrijpen. De video’s zijn een stuk duidelijker en beter dan de meeste video’s op YouTube.

86% van onze leerlingen zegt hoger te scoren.

Een alternatief op dure bijles, altijd uitgelegd door bevoegde docenten.

83% van onze leerlingen zegt onderwerpen sneller te begrijpen.







