Aantal asymmetrische koolstofatomen
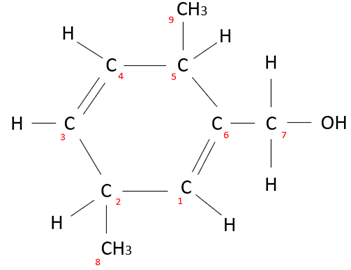
Hieronder is een cyclisch molecuul weergegeven. Geef de nummers van de asymmetrische koolstofatomen en bereken hoeveel spiegelbeeldisomeren het onderstaande molecuul heeft.

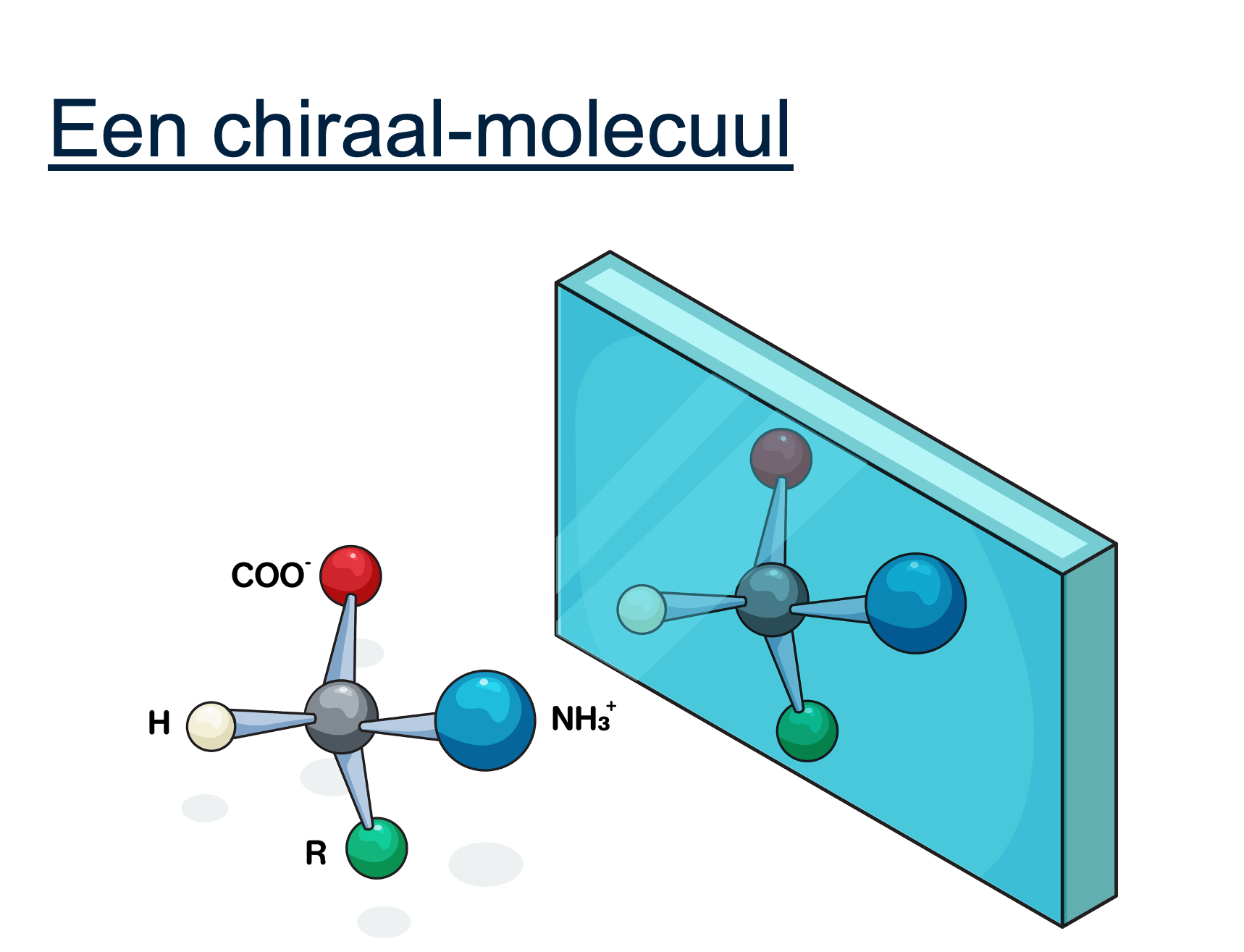
Wel eens gedacht aan de gelijkenis tussen je hand en moleculen? Net zoals je handen niet precies hetzelfde zijn wanneer je ze voor een spiegel houdt, geldt dit ook voor bepaalde moleculen. Dit fenomeen staat bekend als spiegelbeeldisomerie, een intrigerend aspect van de scheikunde dat een grote rol speelt in alles, van de farmaceutische industrie tot de voedingsmiddelenindustrie.
Spiegelbeeldisomerie ontstaat rondom een asymmetrisch koolstofatoom. Dit is een koolstofatoom dat verbonden is met vier verschillende groepen. Stel je een molecuul voor dat één koolstofcentrum heeft met vier uiteenlopende groepen eraan vast. Als je dit molecuul voor een spiegel plaatst en zijn spiegelbeeld probeert na te bouwen, zul je ontdekken dat het origineel en het spiegelbeeld niet op elkaar passen. Dit komt door de specifieke opstelling van de groepen rond het koolstofatoom, wat resulteert in niet-overeenkomende beelden, vergelijkbaar met je linker- en rechterhand.
Het asymmetrische koolstofatoom is de held in het verhaal van spiegelbeeldisomerie. Een eenvoudig voorbeeld hiervan is melkzuur, dat bestaat uit een koolstofatoom in het midden met vier verschillende groepen: een OH-groep, een H-atoom, een zuurgroep en een methylgroep (CH3). Dit roept automatisch spiegelbeeldisomerie op, aangeduid als L(+) en D(-) melkzuur, waarbij de posities van twee groepen worden gewisseld om het spiegelbeeld te vormen.

Hoewel beide isomeren dezelfde fysische eigenschappen zoals kookpunt en dichtheid delen, vertonen ze verschillen in hoe ze interactie aangaan met enzymen in biologische systemen. Dit verschijnsel, bekend als stereospecificiteit, verklaart waarom het ene isomeer door het lichaam kan worden afgebroken en het andere niet. Een klassiek voorbeeld is linksdraaiend melkzuur, dat efficiënter door het menselijk lichaam wordt omgezet dan zijn rechtsdraaiende tegenhanger, vanwege de specifieke pasvorm met enzymen.
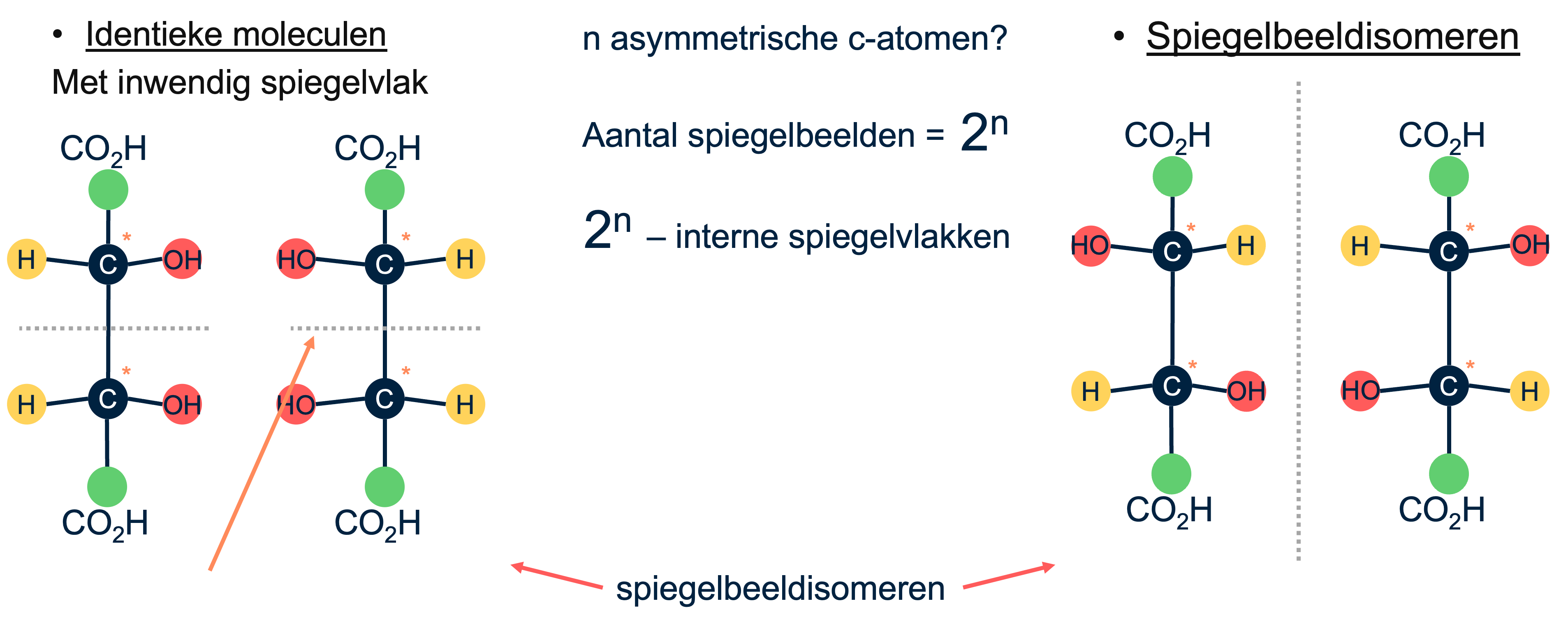
Wanneer een molecuul meer dan één asymmetrisch koolstofatoom bevat, wordt de situatie complexer. Het aantal potentiële spiegelbeeldisomeren neemt toe met de macht van twee per extra asymmetrisch koolstofatoom. Echter, als er een inwendig spiegelvlak bestaat binnen het molecuul, dan reduceert dit het aantal daadwerkelijke unieke spiegelbeeldisomeren. Dit principe is belangrijk voor het begrijpen van complexe moleculaire structuren en hoe deze kunnen leiden tot verschillende chemische eigenschappen en reacties.
We hopen dat deze samenvatting je inzicht heeft gegeven in het concept van spiegelbeeldisomerie en waarom het zo'n cruciaal onderwerp is in de scheikunde. Met deze kennis kun je nu de wondere wereld van moleculen en hun interacties verder verkennen. Veel succes met oefenen!


 Thijs Brouwer
Thijs BrouwerHieronder is een cyclisch molecuul weergegeven. Geef de nummers van de asymmetrische koolstofatomen en bereken hoeveel spiegelbeeldisomeren het onderstaande molecuul heeft.

Spiegelbeeldisomerie: uitleg, samenvatting en oefenen
Krijg de beste uitleg over asymmetrisch koolstofatoom, biochemische selectiviteit, chirale moleculen, intern spiegelvlak, licht polarisatie, links draaiend melkzuur, melkzuur, moleculaire structuur, polarimeter, rechts draaiend melkzuur, spiegelbeeld isomerie, spiegelvlak, stereo specifiek, stereochemie en stereoselectiviteit. Op deze pagina vind je:
Ondersteund door Ainstein, onze AI-hulp die je vragen stap voor stap beantwoordt.
Alle informatie die ik voor mijn toetsen moet kennen is aanwezig, de powerpoints zijn duidelijk en makkelijk te begrijpen. De opdrachten passen altijd goed bij het onderwerp en ondersteunen goed bij het leren. JoJoschool is erg overzichtelijk voor mij!
Ik gebruik het nu voor Biologie, het werkt ontzettend goed, het is heel overzichtelijk en alles wordt behandeld. Hoog rendement haal ik met leren, geen langdradige verhalen, maar ook niet te moeilijk. Het houdt ook automatisch bij hoe ver je bent.
Het is voor mij een erg goede manier om de leerstof voor toetsen te begrijpen. De video’s zijn een stuk duidelijker en beter dan de meeste video’s op YouTube.

86% van onze leerlingen zegt hoger te scoren.

Een alternatief op dure bijles, altijd uitgelegd door bevoegde docenten.

83% van onze leerlingen zegt onderwerpen sneller te begrijpen.







