Wanneer de temperatuur teruggebracht wordt naar nul graden Celsius, zal het volume van methaangas …?
Leerdoelen
•Je kunt uitleggen dat het volume van een mol gas voor alle gassen gelijk is bij constante temperatuur.
•Je kunt rekenen met het molair volume ()
Wet van Avogadro
De wet van Avogadro, genoemd naar de Italiaanse wetenschapper Amedeo Avogadro, stelt dat gelijke volumes van twee verschillende gassen, bij dezelfde druk en temperatuur, hetzelfde aantal deeltjes bevatten. Dit betekent dat bij bijvoorbeeld 0 graden Celsius en 1 atmosfeer druk, 1 liter stikstof hetzelfde aantal moleculen bevat als 1 liter waterstof.
Molaire volumes onder standaardomstandigheden
•Eén mol gas heeft een volume van 22,4 liter bij standaarddruk en 0 graden Celsius. Dit is het molaire volume.
•Bij 25 graden Celsius is het molaire volume 24,5 liter per mol. Dit kun je terugvinden in tabel 7 van de BiNaS.
Het molrekenschema
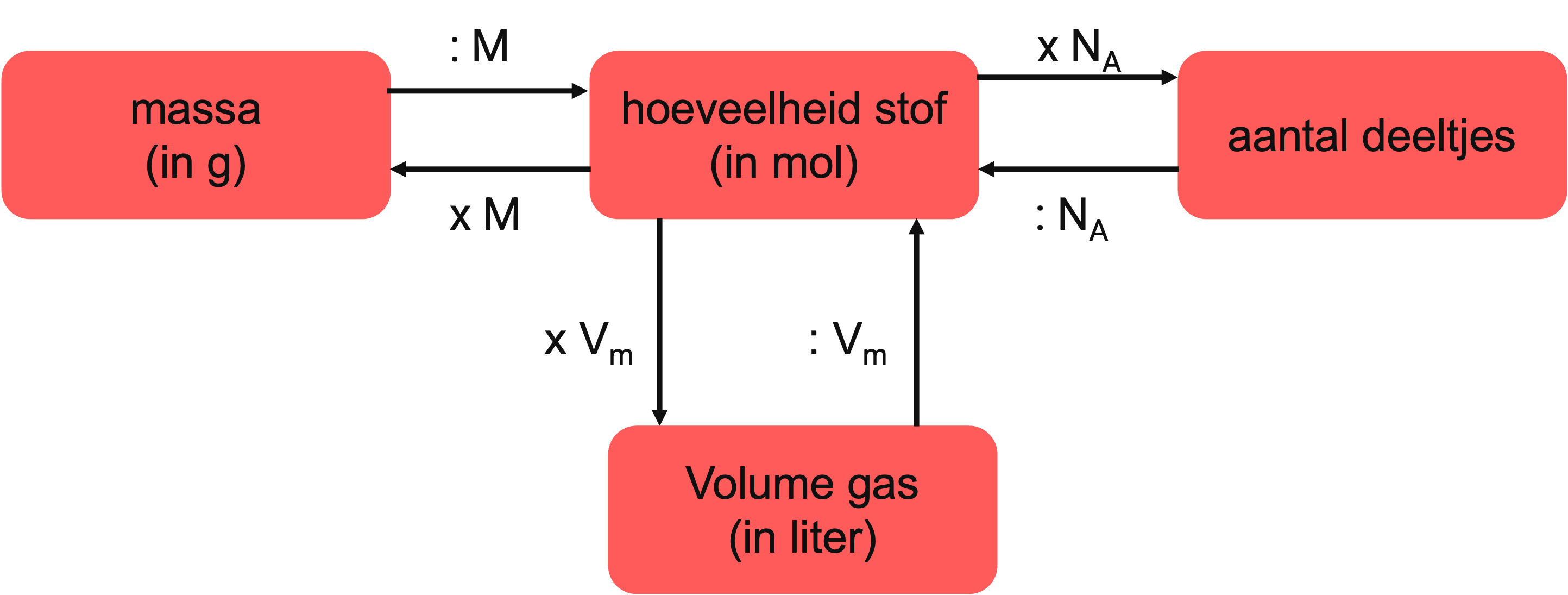
Om te rekenen met gassen, gebruik je het molrekenschema. Dit schema helpt je om van de ene grootheid naar de andere te gaan, zoals van de massa naar het aantal mol of naar het volume van een gas. De M staat voor de molaire massa van de stof. Destaat voor het getal van Avogadro, de hoeveelheid deeltjes die in 1 mol stof zit.staat voor het molaire volume, het volume dat één mol gas inneemt bij bepaalde omstandigheden qua druk en temperatuur.
Rekenvoorbeeld: verbranding van methaanHoeveel literontstaat bij de verbranding van 4,0g methaan bij 25en 1atm?Stap 1: reactievergelijking opstellenStap 2: massa omrekenen naar molDe molaire massa van methaan:Aantal mol methaan:Stap 3: molverhouding gebruikenUit de reactievergelijking:. DusStap 4: mol omrekenen naar volumeBij 25geldtV=n\times V_{m}Dus bij de verbranding van 4,0g methaan bij 25en 1 atm ontstaat 6,1 LIdeale gaswet
Een andere manier om het molaire volume te bepalen, is door gebruik te maken van de ideale gaswet. De ideale gaswet beschrijft het verband tussen de druk, het volume, de temperatuur en de hoeveelheid stof van een ideaal gas. Deze luidt: p\cdot V=n\cdot R\cdot T\to V=\frac{n\cdot R\cdot T}{p}p\cdot V=n\cdot R\cdot T\to V=\frac{n\cdot R\cdot T}{\placeholder{}}p\cdot V=n\cdot R\cdot T\to V=\frac{n\cdot R\cdot}{\placeholder{}}p\cdot V=n\cdot R\cdot T\to V=\frac{n\cdot R}{\placeholder{}}p\cdot V=n\cdot R\cdot T\to V=\frac{n\cdot}{\placeholder{}}p\cdot V=n\cdot R\cdot T\to V=\frac{n}{\placeholder{}}p\cdot V=n\cdot R\cdot T\to V=\frac{\placeholder{}}{\placeholder{}}p\cdot V=n\cdot R\cdot T\to V=p\cdot V=n\cdot R\cdot T\to Vp\cdot V=n\cdot R\cdot T\top\cdot V=n\cdot R\cdot T-p\cdot V=n\cdot R\cdot Tp\cdot V=n\cdot R\cdot T-p\cdot V=n\cdot R\cdot T-\longrightarrow{}p\cdot V=n\cdot R\cdot T-p\cdot V=n\cdot R\cdot Tp\cdot V=n\cdot R\cdot T\longrightarrow{}p\cdot V=n\cdot R\cdot T--p\cdot V=n\cdot R\cdot T-p\cdot V=n\cdot R\cdot Tp\cdot V=n\cdot R\cdotp\cdot V=n\cdot Rp\cdot V=n\cdotp\cdot V=np\cdot V=p\cdot V=Np\cdot V=N\cdotp\cdot V=Np\cdot V=p\cdot Vp\cdotp waarbij:
•p de druk is (in Pascal)
•V het volume is (in kubieke meters)
•n het aantal mol
•R de gasconstante is (8,31 J/(mol·K))
•T de temperatuur is (in Kelvin)
Bepaling molaire volume met de ideale gaswet
Het molaire volume kun je ook zelf afleiden met de ideale gaswet:
Het molaire volume is het volume per mol. Dit betekent
Herschrijven van de ideale gastwet naar
Daarna beide kanten delen door:\rightarrow\larr—
Invullen bij 0(273,15K) en 1 atm:
Omrekenen naar liter:
Eenhedenanalyse
De eenheid van het resultaat is inderdaad een volume, wat blijkt uit de eenhedenanalyse:.














