Waar vindt oxidatie plaats in een autoaccu tijdens stroomlevering?
Leerdoelen
•Je kunt uitleggen waarom een autoaccu oplaadbaar is.
•Je kunt de werking van een loodaccu bij stroomlevering beschrijven.
•Je kunt de werking van een loodaccu bij het opladen beschrijven.
Wat is een elektrochemische cel?
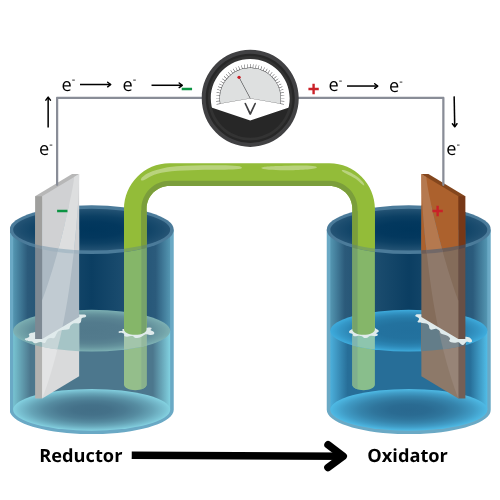
Batterijen, accu's en brandstofcellen worden allemaal aangeduid als elektrochemische cellen. In een elektrochemische cel reageert tijdens stroomlevering altijd de sterkste oxidator aan de pluspool en de sterkste reductor aan de minpool.
Elektronen bewegen van de reductor naar de oxidator, via een externe stroomkring (zoals een lampje of de startmotor van je auto).
•De reductor staat elektronen af (oxidatie). De minpool is de plaats waar dit gebeurt.
•De oxidator neemt elektronen op (reductie). De pluspool is de plaats waar dit gebeurt.
De loodaccu: opbouw en componenten
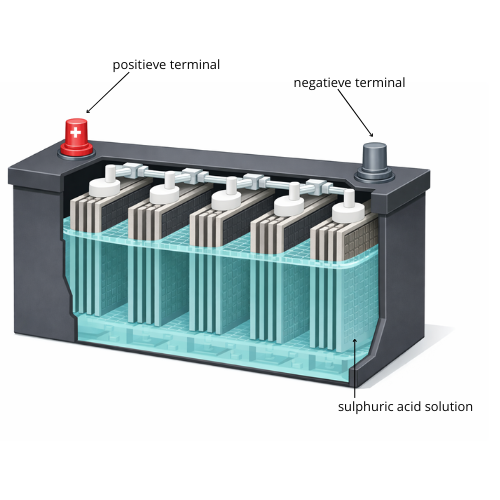
Een typische autoaccu heeft een positieve terminal (pluspool) en een negatieve terminal (minpool). Wat je misschien niet direct ziet, is dat een 12 V loodaccu niet uit één, maar uit meerdere individuele cellen bestaat. Deze cellen zijn in serie geschakeld om de gewenste spanning van 12 V te bereiken. We zullen later zien waarom dit precies zes cellen zijn.
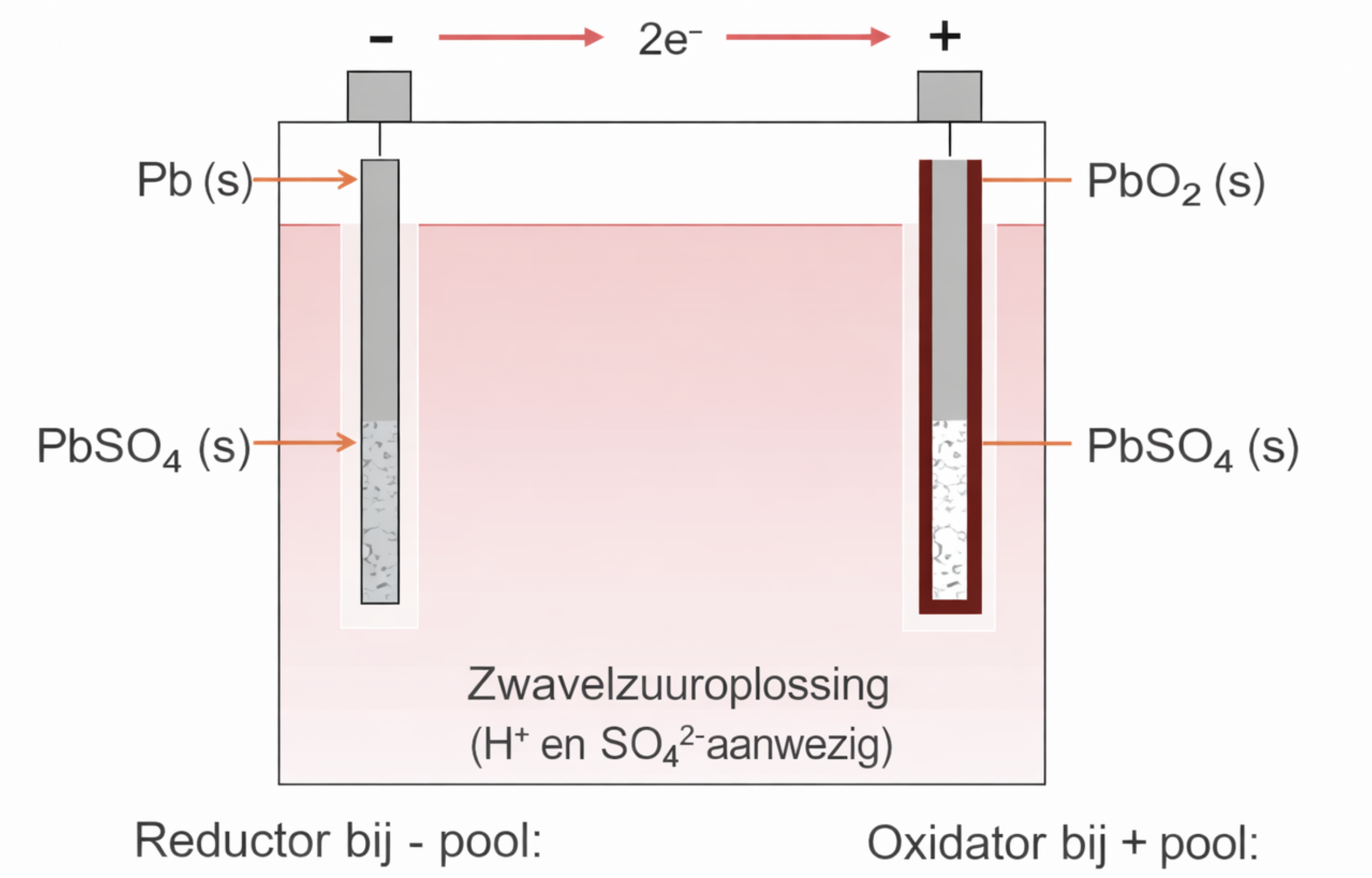
Elektroden en elektrolyt
Binnenin de accu bevinden zich verschillende platen die fungeren als elektroden. De minpool wordt gevormd door platen van zuiver lood (Pb). De pluspool bestaat uit platen van lood met daarop een laagje lood(IV)oxide (). Deze platen zijn ondergedompeld in een oplossing van zwavelzuur (). Deze oplossing, die deen-ionen levert, wordt het elektrolyt genoemd. In dit systeem isde oxidator ende reductor.
Een belangrijke eigenschap van de loodaccu is dat deze oplaadbaar is. Dit komt doordat de reactieproducten die ontstaan tijdens stroomlevering, zowel aan de minpool als de pluspool, vast neerslaan op de elektroden. Het feit dat de reactieproducten als vaste stof op de elektroden neerslaan, maakt het mogelijk om de reactie om te keren.
Werking bij stroomlevering (ontladen)
Wanneer de accu stroom levert, bijvoorbeeld om de motor te starten of de koplampen te laten branden, vinden er aan beide elektroden chemische reacties plaats. Dit zijn redoxreacties, waarbij elektronen worden uitgewisseld.
Reactie aan de minpool (oxidatie)
Aan de minpool, waar het lood (Pb) zich bevindt, treedt de oxidatie op. Het lood reageert met sulfaat-ionen () uit het zwavelzuur. Hierbij ontstaat lood(II)sulfaat () en komen twee elektronen vrij. Deze elektronen worden via de externe stroomkring (de auto) naar de pluspool getransporteerd.
De halfreactie aan de minpool is:
Reactie aan de pluspool (reductie)
Aan de pluspool, waar het lood(IV)oxide () zich bevindt, vindt de reductie plaats. Hier worden de elektronen opgenomen die van de minpool afkomstig zijn. Het lood(IV)oxide reageert met sulfaat-ionen en waterstof-ionen () uit het zwavelzuur, waarbij eveneens lood(II)sulfaat () en water () ontstaan.
De halfreactie aan de pluspool is:
Het belang van neerslag
Zoals je ziet, is lood(II)sulfaat () het reactieproduct aan beide elektroden. Ditis een vaste stof die neerslaat als een wit laagje op de elektroden. Tijdens het ontladen wordt dus zowel de loden plaat als de lood(IV)oxide plaat bedekt met een laagje lood(II)sulfaat. Tegelijkertijd wordenen-ionen uit de oplossing verbruikt, waardoor de concentratie zwavelzuur afneemt.
De bronspanning van een loodaccu berekenen (VWO)
Voor VWO-leerlingen is het mogelijk om de theoretische spanning van een enkele loodaccucel te berekenen met behulp van standaardelektrodepotentialen, die je kunt vinden in Binas-tabel 48.
Let op: in Binas-tabel 48 staan halfreacties altijd als reductie weergegeven. Voor de reactie van de reductor (oxidatie) moet de vergelijking dus van rechts naar links worden gelezen.
Standaardelektrodepotentialen
De bronspanning () van een elektrochemische cel wordt berekend door het verschil tussen de standaardelektrodepotentiaal van de oxidator en die van de reductor.
Deze waarden gelden onder standaardomstandigheden (temperatuur van 298 K en standaarddruk).
In Binas-tabel 48 vind je de volgende waarden voor de relevante redoxkoppels:
•Oxidator ():\text{PbO}_2(s)+\text{SO}_4^{2-}(aq)+4\text{H}^{+}(aq)+2e^{-}\rightleftharpoons\text{PbSO}_4(s)+2\text{H}_2\text{O}(l)\quad V^0=+1{,}69\text{V}
•Reductor (PbSO_4PbSO_{\placeholder{}}PbSOPbSO`PbSO/Pb):\text{PbSO}_4(s)+2e^{-}\rightleftharpoons\text{Pb}(s)+\text{SO}_4^{2-}(aq)\quad V^0=-0{,}36\text{V}
Let op: de reductor is Pb, maar in de tabel zoek je de halfreactie van het redoxkoppel PbSO₄/Pb, waarin Pb de gereduceerde vorm is.
Rekenvoorbeeld
Met deze waarden kunnen we de bronspanning van één cel berekenen:
Een enkele cel van een loodaccu levert dus ongeveer 2,05 V. Aangezien een autoaccu een spanning van 12 V levert, betekent dit dat er 12 V / 2,05 V ≈ 5,85. Omdat het aantal cellen een geheel getal moet zijn, worden er zes cellen in serie geschakeld om de vereiste spanning te bereiken.
Opladen van de loodaccu: het omgekeerde proces
Wanneer een loodaccu leeg is, zijn de elektroden grotendeels bedekt met lood(II)sulfaat () en is de concentratie zwavelzuur in het elektrolyt laag. Om de accu opnieuw te gebruiken, moet deze worden opgeladen.
Opladen houdt in dat we een externe elektrische stroom door de accu sturen, in de tegenovergestelde richting van de stroomlevering. Dit kan via een acculader (die je aansluit op het stopcontact) of door startkabels te gebruiken met een andere, werkende accu. Het is cruciaal om de pluspool van de lader/andere accu met de pluspool van jouw accu te verbinden, en de minpool met de minpool. Een omgekeerde aansluiting kan ernstige schade veroorzaken.
Omgekeerde reacties
De externe stroom dwingt de chemische reacties om in omgekeerde richting te verlopen, waardoor de oorspronkelijke stoffen worden hersteld. Hierbij vindt aan de minpool reductie plaats en aan de pluspool oxidatie, wat het omgekeerde is van het proces bij stroomlevering.
•Aan de minpool: Het neergeslagen lood(II)sulfaat () neemt elektronen op en wordt weer omgezet in zuiver lood (Pb) en sulfaat-ionen ().
•Aan de pluspool: Het lood(II)sulfaat () wordt samen met water omgezet in lood(IV)oxide (), sulfaat-ionen (), waterstof-ionen () en er komen elektronen vrij die terugstromen naar de externe stroombron.














