Welke uitspraak is juist?
Leerdoelen
•Je kunt uitleggen welke van de twee, de reductor of de oxidator, gekoppeld is aan de pluspool en welke aan de minpool in een elektrochemische cel.
•Je kunt globaal de werking van een staafbatterij uitleggen.
•Je kunt de locatie van de minpool in een staafbatterij aanwijzen aan de hand van een afbeelding.
•Je kunt verklaren waarom een staafbatterij niet oplaadbaar is.
De elektrochemische cel
Batterijen, accu's en brandstofcellen zijn allemaal voorbeelden van elektrochemische cellen. Dit zijn apparaten die chemische energie omzetten in elektrische energie (stroom) via redoxreacties, of andersom.
Plaats van de reductor en de oxidator
De reductor reageert aan de minpool en staat daarbij elektronen af. Hierdoor ontstaat bij de minpool een overschot aan elektronen, waardoor deze negatief geladen is.
De oxidator neemt elektronen op. Bij de pluspool worden elektronen verbruikt, waardoor daar een tekort aan elektronen ontstaat. Hierdoor is de pluspool positief geladen.
Door dit verschil in lading bewegen elektronen via de externe stroomkring van de minpool naar de pluspool.
De staafbatterij: een zink-koolstofcel
De meestvoorkomende staafbatterij, zoals die van het Duracell-konijntje, wordt ook wel de zink-koolstofcel genoemd. Deze batterij genereert stroom door chemische reacties waarbij zink en koolstof een belangrijke rol spelen.
Opbouw van de zink-koolstofcel
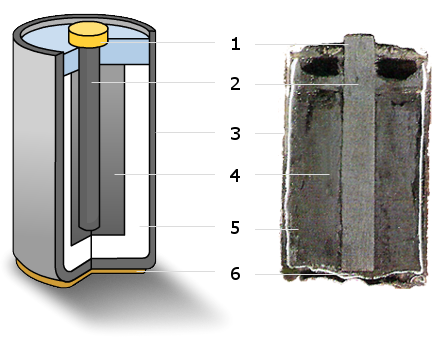
De verschillende onderdelen zijn:
1.De pluspool: Dit is de gele knop aan de bovenkant van de batterij. Hier komen de elektronen vanuit de externe stroomkring de batterij weer binnen.
2.De grafietstaaf: Direct onder de pluspool bevindt zich een donkere grafietstaaf. Deze is gemaakt van koolstof (vergelijkbaar met de binnenkant van een potlood) en vormt de positieve elektrode (pluspool). Aan het oppervlak van deze staaf vindt de reductiereactie plaats.
3.Het zinken omhulsel: Dit is de buitenkant van de batterij, vaak herkenbaar aan de metalen glans. Het zinken omhulsel fungeert in zijn geheel als de minpool van de batterij.
4.Bruinsteen (): Rondom de grafietstaaf bevindt zich een donkere massa, bruinsteen. Dit is de stof mangaan(IV)oxide (). Dit is de oxidator in de batterij.
5.Het elektrolyt: Dit is het witte deel dat de ruimte tussen de grafietstaaf/bruinsteen en het zinken omhulsel opvult. Het elektrolyt is een oplossing met geladen deeltjes (ionen), die zich binnen de batterij kunnen verplaatsen. Het heeft een vergelijkbare functie als een zoutbrug in andere elektrochemische cellen: het zorgt voor ladingsbalans, doordat ionen kunnen bewegen om de ladingsverschillen die ontstaan door het elektronenverkeer te compenseren.
6.De minpool: De onderkant van het zinken omhulsel vormt het externe contactpunt van de minpool. Via dit punt verlaten de elektronen de batterij de externe stroomkring in.
De redoxreacties in de staafbatterij
De werking van de batterij is gebaseerd op twee halfreacties: één bij de minpool (oxidatie) en één bij de pluspool (reductie).
Bij de minpool: oxidatie van zink
Het zinken omhulsel (de minpool) dient als de reductor. Zinkatomen (Zn) geven elektronen af en worden omgezet in zinkionen ().
Deze elektronen ontstaan dus aan de buitenkant van de batterij (het zinken omhulsel).
Bij de pluspool: reductie van mangaan(IV)oxide
Aan de pluspool reageert mangaan(IV)oxide () als oxidator. Het neemt de elektronen op die via de externe stroomkring worden aangevoerd. Hierbij is ook water nodig, dat afkomstig is uit het vochtige elektrolyt. Hierbij ontstaan dimangaantrioxide () en hydroxide-ionen ().
Elektronenstroom en stroomkring
De elektronen die aan de minpool worden afgegeven, bewegen van de minpool naar de pluspool. Ze kunnen echter niet direct door het elektrolyt. Ze moeten via een externe stroomkring bewegen. Dit betekent dat je de minpool met een draadje moet verbinden met de pluspool, en daar eventueel een apparaatje (zoals een lampje) tussen moet plaatsen. Pas dan gaat de batterij werken en levert ze stroom. De elektronen verlaten het zinken omhulsel, gaan door het lampje, en komen aan bij de grafietstaaf waar ze door de oxidator worden opgenomen.
Waarom een staafbatterij niet oplaadbaar is
In theorie zou je een redoxreactie omgekeerd kunnen laten verlopen door middel van elektrolyse, oftewel door er stroom op te zetten (zoals je je telefoon oplaadt via het stopcontact). Echter, een zink-koolstofcel is niet oplaadbaar. Dit komt doordat de gevormde stoffen tijdens het ontladen niet op de elektroden blijven zitten. Dit geldt met name voor de reactie aan de minpool:.
Wanneer een zinkatoom elektronen afgeeft en een-ion wordt, blijft dit ion niet aan de elektrode (het zinken omhulsel) vastzitten. Omdateen ion is, kan het gemakkelijk bewegen. Dit ion diffundeert weg van de minpool en lost op in het elektrolyt. Zodra de zinkionen zijn opgelost in het elektrolyt en weg zijn van de minpool, kunnen ze niet meer gemakkelijk teruggebracht worden tot hun oorspronkelijke vaste vorm op de elektrode door simpelweg de stroomrichting om te keren.
Bij een auto-accu, die wel oplaadbaar is, slaan de gevormde stoffen juist wel neer op de elektroden en blijven ze daar, waardoor de reactie omkeerbaar is. Bij de zink-koolstofcel gebeurt dit niet, en daarom kun je deze batterij niet opladen.














