Welke deeltjes bewegen door het membraan in een brandstofcel?
Leerdoelen
•Je kunt het verschil tussen een batterij en een brandstofcel uitleggen.
•Je kunt benoemen welke stof altijd de oxidator is in een brandstofcel.
•Je kunt beschrijven hoe-ionen (protonen) door het membraan van een brandstofcel bewegen.
Wat is een brandstofcel?
Een brandstofcel is een elektrochemisch apparaat dat, net als een batterij, chemische energie direct omzet in elektrische energie. Het grote verschil met een batterij is dat een brandstofcel constant van buitenaf brandstof en een oxidator aangevoerd krijgt, terwijl de reactanten in een batterij al opgeslagen zijn en opraken. Dit betekent dat een brandstofcel theoretisch onbeperkt stroom kan leveren zolang er brandstof en zuurstof beschikbaar zijn.
Algemene principes: reductor en oxidator
Bij een elektrochemische reactie zijn altijd een reductor en een oxidator betrokken:
•De reductor staat elektronen af en reageert bij de minpool.
•De oxidator neemt elektronen op en reageert bij de pluspool.
De componenten van een brandstofcel
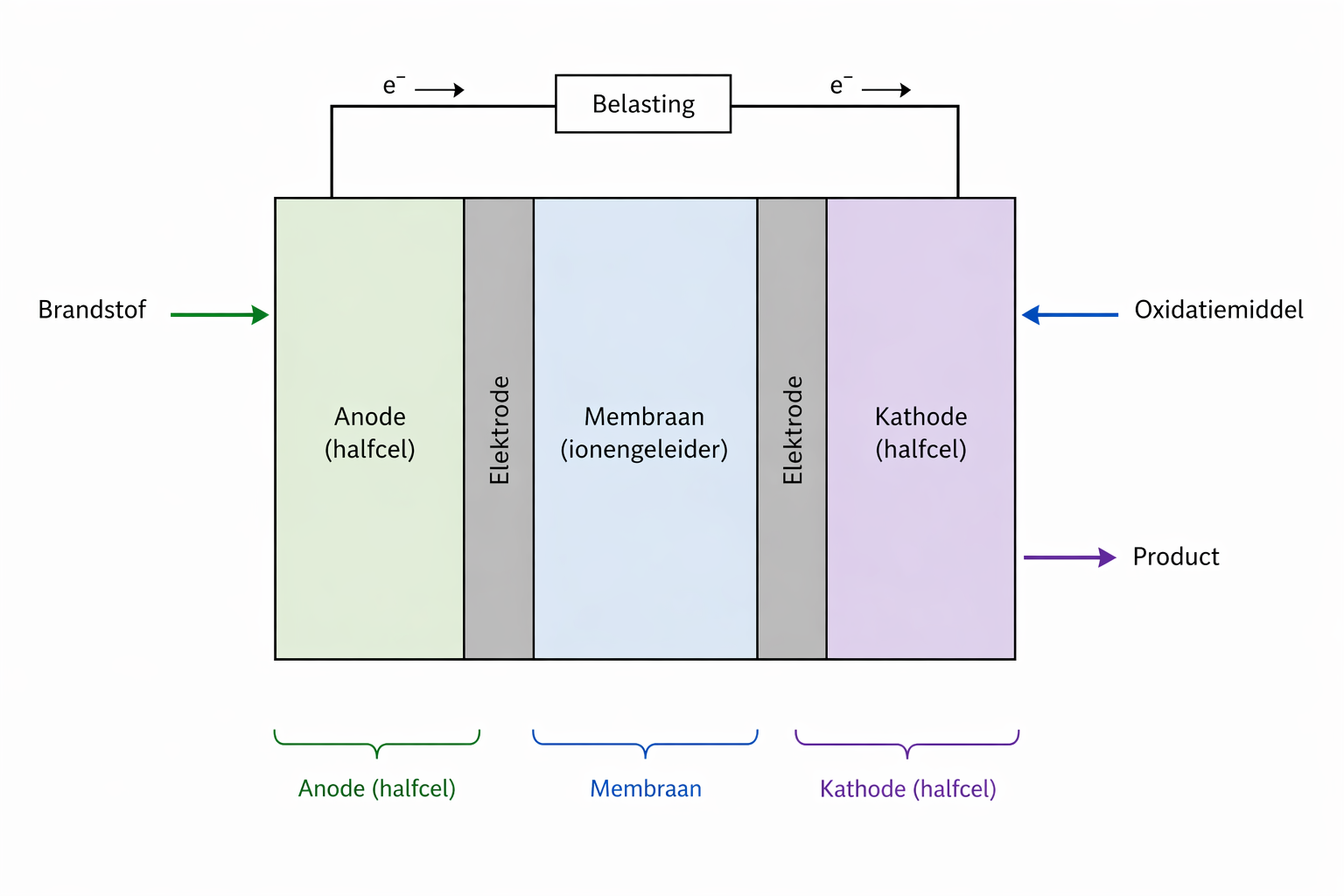
Een brandstofcel bestaat uit twee gescheiden ruimtes, de halfcellen, en een membraan.
•Halfcellen: In de ene halfcel bevindt zich de oxidator, in de andere de reductor.
•Membraan: Een membraan scheidt de twee halfcellen. Dit membraan is cruciaal, omdat het alleen bepaalde deeltjes doorlaat, zoals-ionen, maar geen elektronen. Dit zorgt ervoor dat de elektronen via een externe stroomkring moeten lopen, waardoor er elektriciteit ontstaat.
De reactanten in een brandstofcel
In elke brandstofcel zijn de rollen van de oxidator en de brandstof (reductor) duidelijk verdeeld.
De oxidator: zuurstof
De stof die altijd de oxidator is in een brandstofcel, ongeacht de brandstof die wordt gebruikt, is zuurstof (). Dit is logisch, want zuurstof is een zeer goede oxidator en is overal in ruime mate aanwezig (denk aan lucht). Zuurstof wordt daarom continu aangevoerd en reageert aan de pluspool van de brandstofcel.
De brandstof: koolwaterstoffen als reductor
De brandstof in een brandstofcel is vaak een koolwaterstof, of een stof die hierop lijkt. Koolwaterstoffen zijn organische verbindingen die bestaan uit koolstof- (C) en waterstof- (H) atomen, en soms ook zuurstof- (O) atomen. Voorbeelden zijn:
•methaan ()
•ethaan ()
•propaan ()
•glucose ()
•methanol ()
Deze brandstoffen fungeren als de reductor en reageren aan de minpool van de brandstofcel. Net als bij normale verbranding, waarbij koolwaterstoffen met zuurstof reageren enenvrijkomen met warmte, vinden in de brandstofcel soortgelijke reacties plaats. Het grote verschil met een normale verbranding is dat de chemische energie niet als warmte vrijkomt, maar direct wordt omgezet in elektrische energie.
Werking van een methanolbrandstofcel
Laten we de werking van een brandstofcel toelichten aan de hand van een voorbeeld met methanol () als brandstof.
De opbouw
In een methanolbrandstofcel wordt methanol, vaak samen met water, aan de ene zijde (de reductor-halfcel) aangevoerd. Aan de andere zijde (de oxidator-halfcel) wordt zuurstof aangevoerd (bijvoorbeeld uit de lucht). Aan de reductorzijde ontstaat koolstofdioxide () als afvalproduct en aan de oxidatorzijde ontstaat water ().
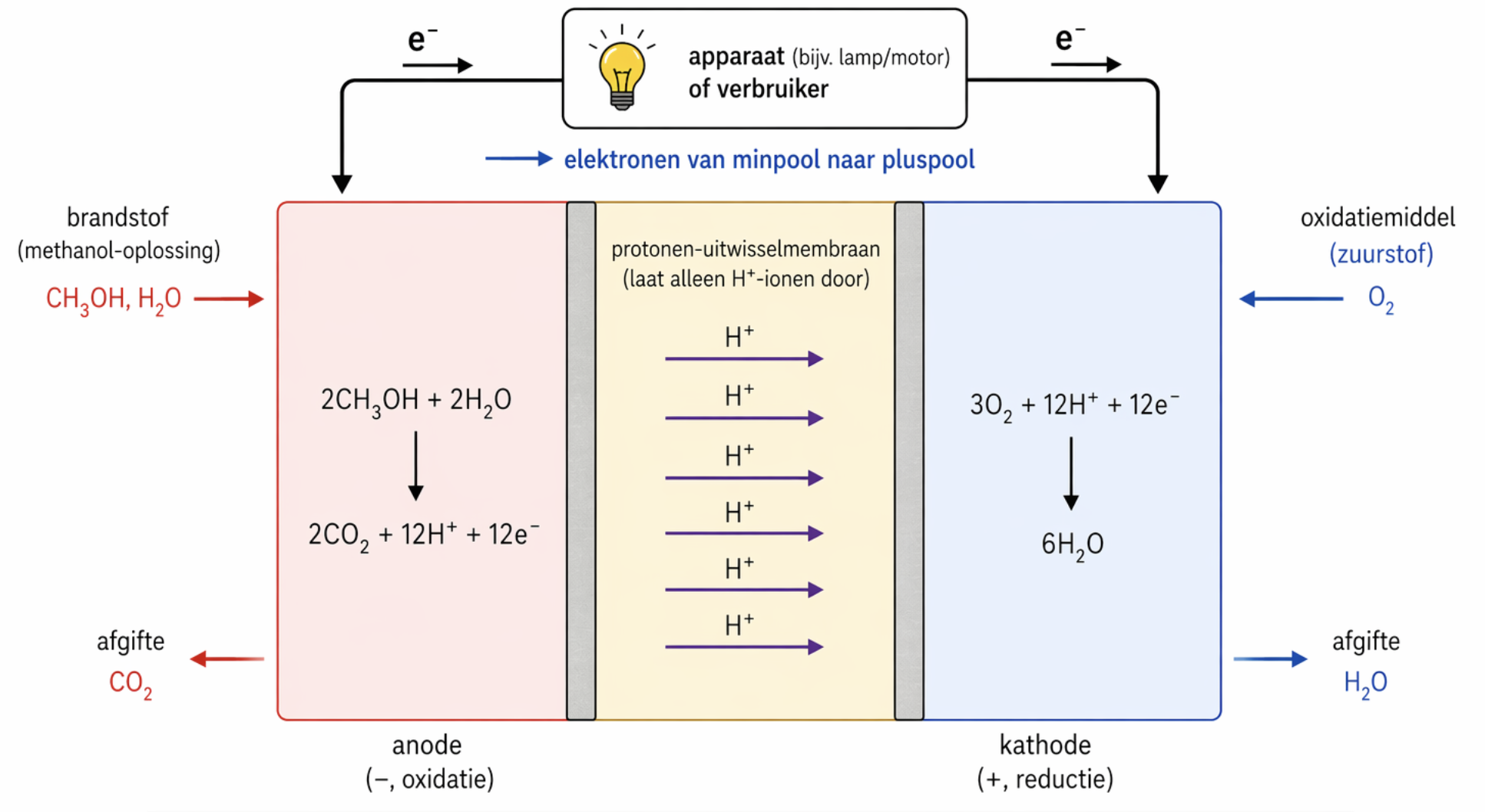
De halfreacties
Om de totale reactie in de brandstofcel te begrijpen, kijken we naar de twee halfreacties:
1.Oxidator halfreactie (bij de pluspool): Zuurstof reageert hier. Deze reactie is (bijna) altijd hetzelfde in brandstofcellen en is te vinden in Binas tabel 48. Hierin neemt zuurstof elektronen en-ionen op om water te vormen.
1.Reductor halfreactie (bij de minpool): De brandstof reageert hier, in dit geval methanol. De elektronen staan rechts van de pijl, wat aangeeft dat het een oxidatie is (elektronen worden afgestaan). Je hoeft deze vergelijking niet zelf te bedenken, maar je moet hem mogelijk kloppend kunnen maken als je extra informatie krijgt.
Hierbij wordt methanol omgezet in koolstofdioxide, waarbij-ionen en elektronen vrijkomen.
Het combineren van halfreacties: de totaalreactie
Om de complete totaalreactie van de brandstofcel te krijgen, moeten we de twee halfreacties optellen. Hierbij moet het aantal elektronen aan beide zijden van de totale reactie gelijk zijn, zodat ze tegen elkaar wegvallen.
•De oxidator halfreactie heeft 4 elektronen.
•De reductor halfreactie heeft 6 elektronen.
Om het aantal elektronen gelijk te maken, vermenigvuldigen we de bovenste reactie met 3 en de onderste met 2:
1.
2.
Nu tellen we deze twee vergelijkingen bij elkaar op:
We strepen de deeltjes die aan beide kanten van de pijl staan tegen elkaar weg (12-ionen en 12 elektronen). Ook de 2aan de linkerkant van de tweede reactie kunnen we wegstrepen tegen de 6aan de rechterkant van de eerste reactie (er blijven dan 4aan de rechterkant over).
De totaalreactie wordt:
Deze totaalreactie is in feite de volledige verbranding van methanol. Dit illustreert dat brandstofcellen de verbranding van een brandstof gebruiken om direct elektriciteit op te wekken.
Je kunt dit principe ook toepassen op andere brandstoffen. Stel dat je glucose () in een brandstofcel stopt, dan zal de totaalreactie ook een verbrandingsreactie zijn:
De cruciale rol van het membraan
Het membraan speelt een sleutelrol in de brandstofcel door de scheiding van-ionen en elektronen te faciliteren, wat de productie van elektriciteit mogelijk maakt.
H⁺-ionen door het membraan
De-ionen (protonen) die ontstaan aan de reductorzijde (bijvoorbeeld uit de methanolreactie:) zijn klein genoeg om door het speciale membraan te bewegen. Ze bewegen van de reductor-halfcel naar de oxidator-halfcel. Daar worden ze gebruikt door de zuurstof om samen met de elektronen water te vormen.
Elektronen door de externe stroomkring
De elektronen die vrijkomen aan de reductorzijde kunnen echter niet door het membraan heen. Ze worden gedwongen om via een externe stroomkring te reizen. Deze elektronenstroom kan worden gebruikt om bijvoorbeeld een elektromotor of een ander apparaat van stroom te voorzien. Nadat ze arbeid hebben verricht, komen de elektronen aan bij de pluspool (oxidator-halfcel), waar ze samen met de-ionen en zuurstof reageren tot water.














