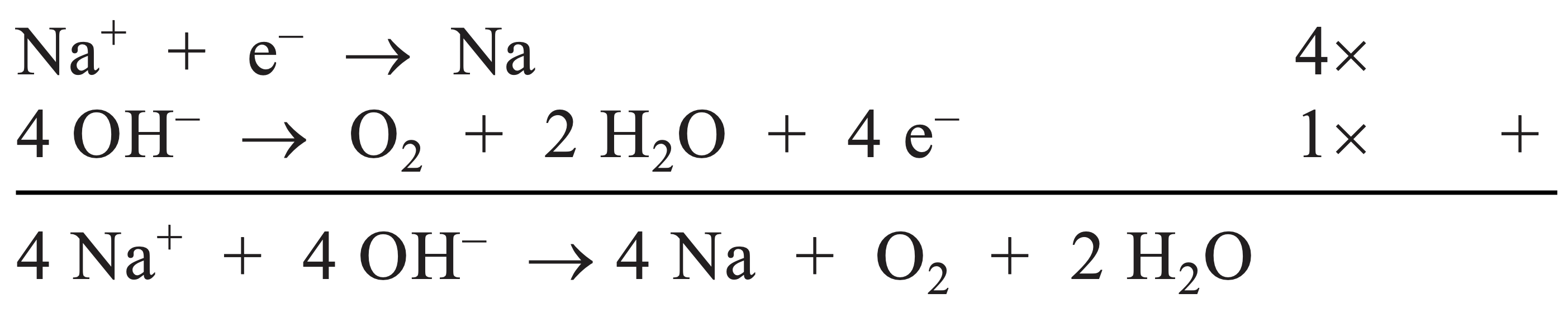De huidige lithium-ionbatterij is geschikt voor de duurzame opslag van energie, maar het benodigde lithium is schaars. Daarom wordt onderzoek gedaan naar een accu die natrium-ionen gebruikt.$\mathrm{Na}^{+}-ionen zijn overvloedig aanwezig in zeewater. De molariteit van de$\mathrm{Na}^{+}-ionen hierin is gemiddeld 470 mmol per liter zeewater.
- Oefen examens van de afgelopen 5 jaar met extra uitleg door docenten bij examenvragen
- Extra uitleg en oefenen voor elk onderwerp uit je examen
- Stel vragen en krijg direct antwoord

Bij het opladen vindt aan de natriumelektrode een halfreactie plaats waarbij$\mathrm{Na}^{+}-ionen uit oplossing A worden omgezet tot natrium.
Zeewater is licht basisch. Aan de koolstofelektrode reageren bij het opladen hydroxide-ionen tot zuurstof en water volgens halfreactie 1.
opladen:$\quad 4 \mathrm{OH}^{-} \rightarrow \mathrm{O}_{2}+2 \mathrm{H}_{2} \mathrm{O}+4 \mathrm{e}^{-}(halfreactie 1)
•Geef de halfreactie die aan de natriumelektrode plaatsvindt bij het opladen.
•Leid de totale vergelijking af van de reacties bij het opladen.
Op deze pagina behandelen we vraag 11 van het centraal examen scheikunde havo 2025 – tijdvak 2. Deze vraag is onderdeel van Zeewater-accu, en is 2 punten waard.
Je kunt hier zelf het antwoord invullen en vervolgens direct de uitwerking en uitleg bekijken.
Daarnaast kun je:
- Oude antwoorden terugzien
- Extra uitleg vragen aan onze AI-hulp via de knop "Stel je vraag"
- Klikken op de bijbehorende onderwerpen uit de examenroute om verdieping te vinden