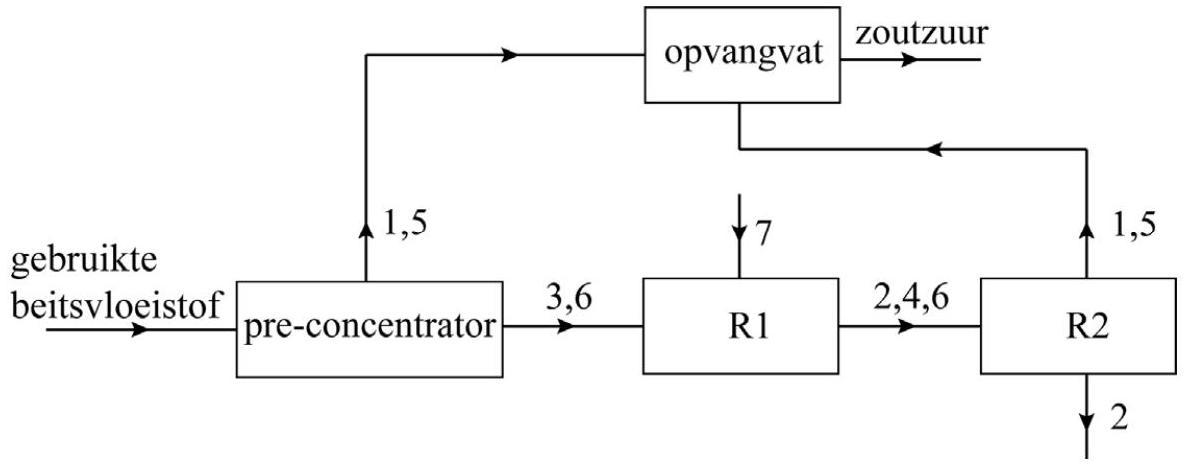
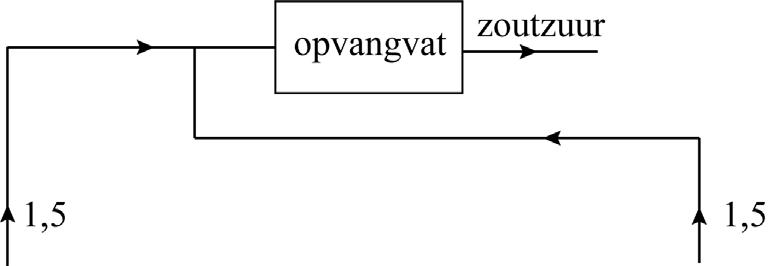
Bij het maken van plaatstaal wordt beitsvloeistof gebruikt. Na gebruik bevat deze waterige vloeistof\mathrm{Fe}^{2+}\text{-ionen}$\mathrm{Fe}^{2+},\mathrm{H}^{+}\text{-ionen}$\mathrm{H}^{+}en\mathrm{Cl}^{-}\text{-ionen}$\mathrm{Cl}^{-}. In deze opgave worden twee processen beschreven waarmee gebruikte beitsvloeistof wordt gerecycled: het proces van New Zealand Steel (proces A) en het proces van SMS Siemag (proces B). In beide processen wordt gebruikte beitsvloeistof omgezet tot onder andere\mathrm{Fe}^{3+}\text{-ionen}\mathrm{Fe}^{3+}\mathrm{Fe}^{3+}\mathrm{Fe}^{3+}\mathrm{Fe}^{3+}\mathrm{Fe}^{3+}\mathrm{Fe}^{3+}\mathrm{Fe}^{3+}\mathrm{Fe}^{3+}\mathrm{Fe}^{3+}\mathrm{Fe}^{3+}\mathrm{Fe}^{3+}\mathrm{Fe}^{3+}\mathrm{Fe}^{3+}$\mathrm{Fe}^{3+}\mathrm{Fe}^{3+}ProcesBHetprocesvanSMSSiemagvindtplaatsindriestappenenisopdeuitwerkbijlageonvolledigenschematischweergegeven:Stap1:Degebruiktebeitsvloeistofwordtverwarmdtotineenpre-concentrator.Hierdoorverdampteendeelvanhetwatereneendeelvanhetopgeloste.Dezegassenwordennaareenopvangvatgeleid.Eengeconcentreerdeoplossingvan,enstroomtnaarreactor1(R1).Stap2:InR1reagerenalle-ionenmetzuurstofvolgensreactie2,bijeentemperatuurvaneneendrukvan7bar.Stap3:Deontstanesuspensiewordtinreactor2(R2)geleidbijeentemperatuurvan.Hierverdamptnogmeerwater.Ooktreedtreactie3op:VastwordtonderinR2afgevoerdenopgeslagen.AlleoverigeenverlatenR2als.Allegasvormigestoffenwordennaarhetopvangvatgeleid.$\mathrm{Fe}^{3+}en \mathrm{HCl}_{}\text{-gas}\mathrm{HCl}_{}\mathrm{HCl}_{}\mathrm{HCl}_{}\mathrm{HCl}_{}\mathrm{HCl}_{}\mathrm{HCl}_{}\mathrm{HCl}_{}\mathrm{HCl}_{}\mathrm{HCl}_{}\mathrm{HCl}_{}\mathrm{HCl}_{}.
Proces A
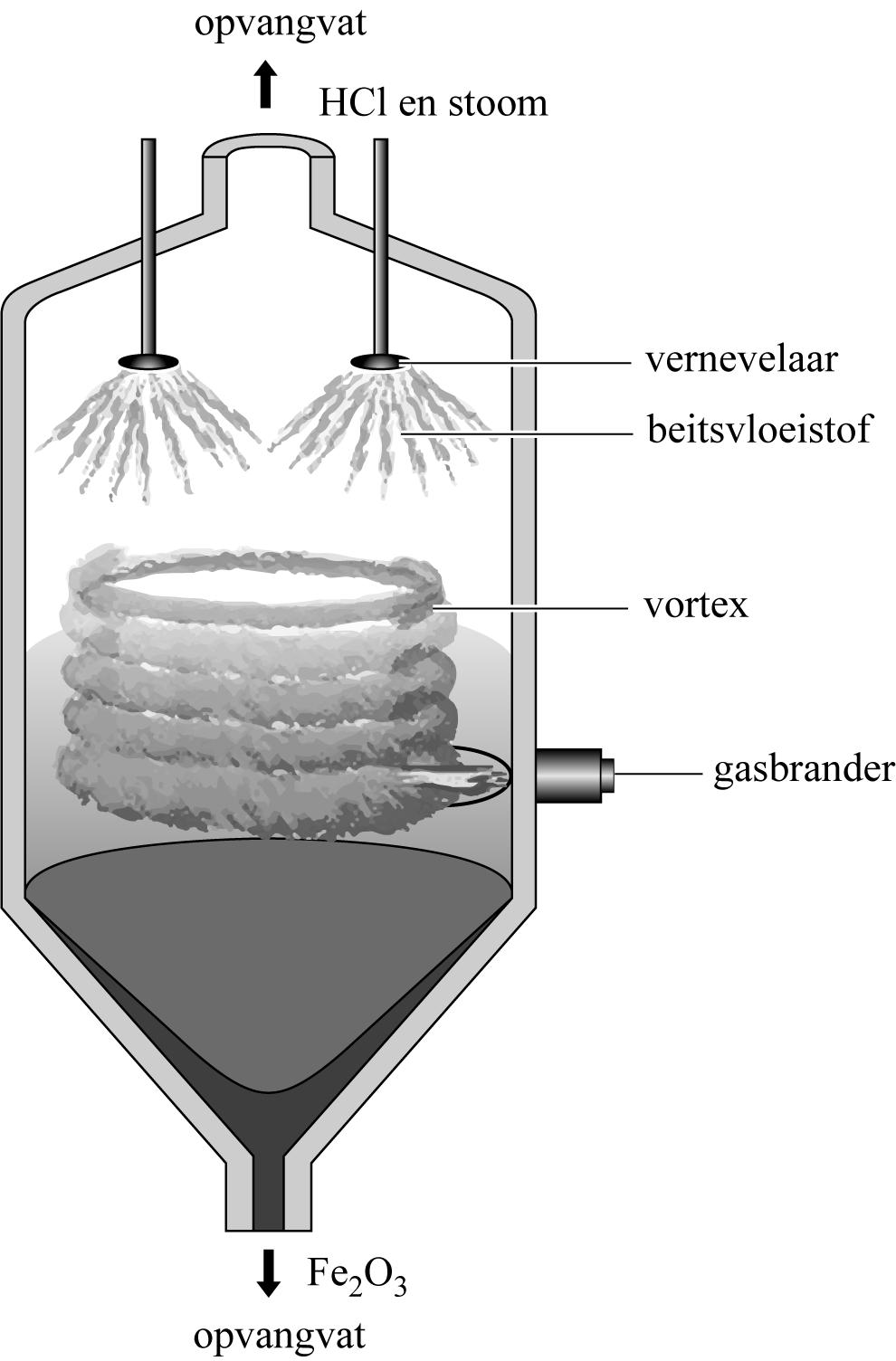
Het bedrijf New Zealand Steel maakt gebruik van een vortexreactor. Zie figuur 1. Een vortexreactor is een reactor waarin een ronddraaiende stroom van gassen (een vortex) aanwezig is. De reactor wordt verwarmd met behulp van gasbranders. De gebruikte beitsvloeistof wordt via vernevelaars van boven in de reactor gebracht bij een temperatuur van minimaal350\ \degree\text{C}350\ \degree350\ \degree350\ \degree350\ \degree350\ \degree350\ \degree350\ \degree350\ \degree350\ \degree350\degree350\degree350\degree350350350350350350350350350^{}350^{\circ}350^{\circ}\mathrm{C}350^{\circ}\mathrm{C}350^{\circ}\mathrm{C}$350^{\circ} \mathrm{C}. Hierdoor verdampt het water waarin de ionen zijn opgelost en ontstaan vast$\mathrm{FeCl}_{2}en gasvormig\mathrm{HCl}_{}\mathrm{CHCl}_{}\mathrm{CHCl}_2\mathrm{CHl}_2\mathrm{Cl}_2H\mathrm{Cl}_2. Het vaste$\mathrm{FeCl}_{2}reageert vervolgens in de vortexreactor tot$\mathrm{Fe}_{2} \mathrm{O}_{3}, wat aan de onderkant van de reactor wordt afgevoerd en opgeslagen.en stoom verlaten de vortexreactor aan de bovenkant en worden opgevangen.