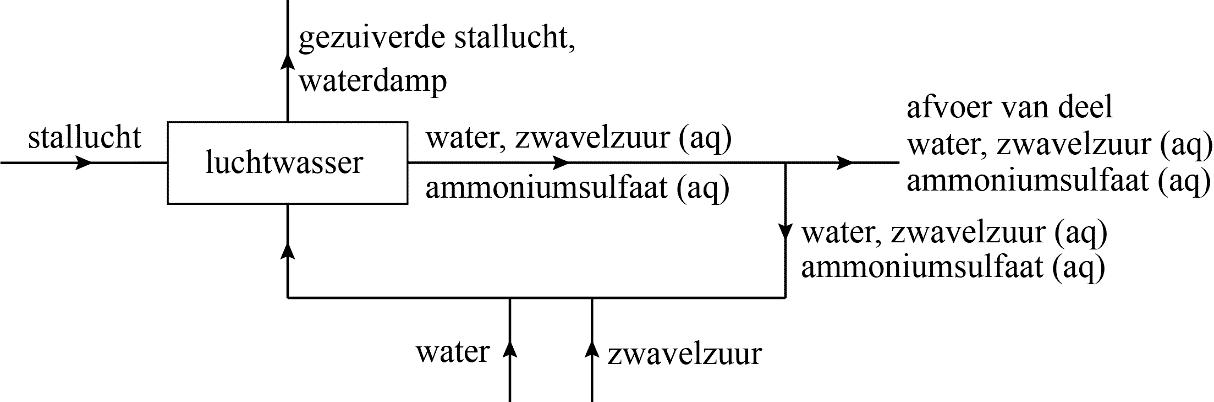
Voorbeelden van een juiste berekening zijn:
Er moet$\frac{1{,}0 \cdot 10^{3}}{17{,}0}=58{,}8(\mathrm{mol}) \mathrm{NH}_{3}worden omgezet.
Het aantal$\mathrm{mol} \mathrm{H}_{2} \mathrm{SO}_{4}dat nodig is, bedraagt:$\frac{58{,}8}{2}=29{,}4.
De massa van$\mathrm{H}_{2} \mathrm{SO}_{4}die nodig is, bedraagt:$29{,}4 \times 98{,}1=2{,}89 \cdot 10^{3}(\mathrm{g}).
Het benodigde volume van$\mathrm{H}_{2} \mathrm{SO}_{4}is dus$\frac{2{,}89 \cdot 10^{3}}{1{,}84 \cdot 10^{3}}=1{,}6(\mathrm{dm}^{3}).
(1{,}6\mathrm{dm}^3$(1{,}6 \mathrm{dm}^{3}\right.is nagenoeg$\left.1{,}5 \mathrm{~L})
➤ Indien correct 1 punt:
➤ Indien correct 1 punt:
➤ Indien correct 1 punt:
➤ Indien correct 1 punt:
of
$1{,}5 \mathrm{~L} \mathrm{H}_{2} \mathrm{SO}_{4}heeft een massa van$1{,}5 \times 1{,}84 \cdot 10^{3}=2{,}76 \cdot 10^{3}(\mathrm{g}).
Dit komt overeen met$\frac{2{,}76 \cdot 10^{3}}{98{,}1}=28{,}1(\mathrm{mol}) \mathrm{H}_{2} \mathrm{SO}_{4}.
Hiermee wordt$28{,}1 \times 2=56{,}3(\mathrm{mol}) \mathrm{NH}_{3}omgezet.
Dat is$56{,}3 \times 17{,}0 \times 10^{-3}=9{,}6 \cdot 10^{-1}(\mathrm{~kg})of$56{,}3 \times 17{,}0=9{,}6 \cdot 10^{2}(\mathrm{g}).
(9{,}6\cdot10^{-1}\mathrm{~kg}(9{,}6\cdot10^{-1}\mathrm{~k}(9{,}6\cdot10^{-1}\mathrm{~kg}(9{,}6\cdot10^{-1}\mathrm{~kg}\right$(9{,}6 \cdot 10^{-1} \mathrm{~kg}\right.is nagenoeg$1{,}0 \mathrm{~kg}.)
➤ Indien correct 1 punt:
➤ Indien correct 1 punt:
➤ Indien correct 1 punt:
➤ Indien correct 1 punt: