In veel mobiele telefoons zit een lithium-ionbatterij. Deze batterijen zijn licht, kunnen veel energie leveren en zijn snel op te laden. Het basisontwerp van een lithium-ionbatterij is in figuur 1 schematisch weergegeven.
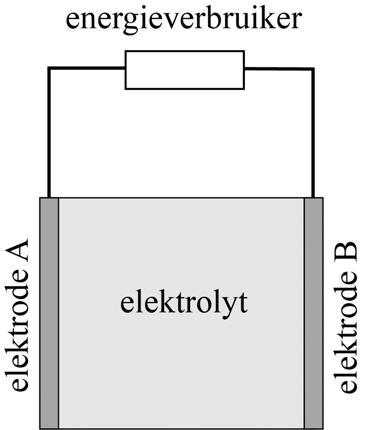
Elektrode A bevat onder andere het metaal lithium (Li). Elektrode B bevat$\mathrm{Li}^{+}-ionen. Tussen beide elektroden bevindt zich een elektrolyt, dat bestaat uit een polymeer waarin zich een vloeibaar lithiumzout bevindt.
Een veelgebruikt polymeer is PEO. De formule van PEO is$(\mathrm{CH}_{2} \mathrm{CH}_{2} \mathrm{O})_{n}.
In figuur 2 is een vergroting van het elektrolyt schematisch weergegeven.
Hierin is te zien hoe een$\mathrm{Li}^{+}-ion van polymeerketen naar polymeerketen wordt doorgegeven, doordat telkens een ander groepje O-atomen het$\mathrm{Li}^{+}-ion bindt. De binding komt tot stand doordat de O-atomen in PEO enigszins negatief geladen zijn. Dit is het gevolg van een polaire atoombinding tussen de C-atomen en de O-atomen in PEO. Tijdens de stroomlevering bewegen$\mathrm{Li}^{+}-ionen van elektrode A naar elektrode B.

