Wat is het belangrijkste verschil tussen een ontleding en een verbranding?
Leerdoelen
•Je kunt beschrijven wat er gebeurt bij een chemische reactie.
•Je kunt een reactieschema opstellen van een ontleding.
•Je kunt een reactieschema opstellen van een verbranding.
•Je kunt de zeven reactieverschijnselen benoemen.
Ontleden
Bij ontleden valt een molecuul uit elkaar. Dit kun je vergelijken met een bouwwerkje van Lego. Je hebt verschillende LEGO-steentjes die samen één bouwproduct (het molecuul) maken. Als je dit bouwwerkje uit elkaar haalt, hou je alleen de losse steentjes (de elementen of atomen) over. Dit proces heet ontleden.
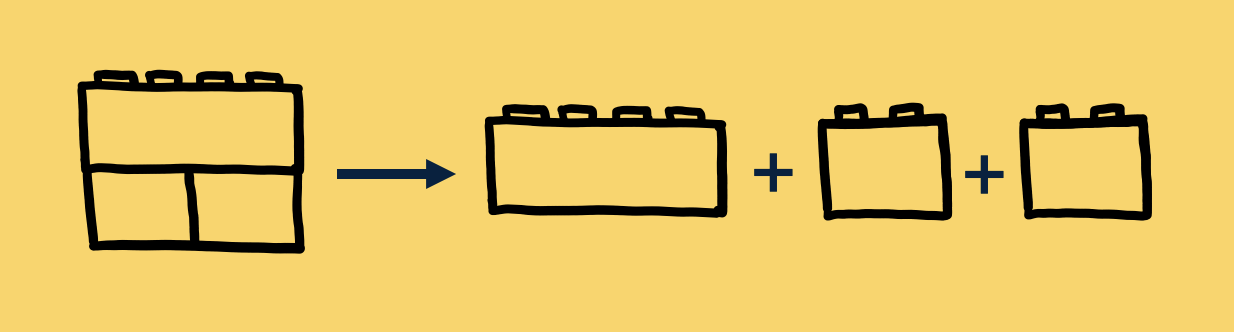
Een reactieschema maken voor ontleden
Ontleden kun je opschrijven in een reactieschema. Zo'n schema ziet er altijd als volgt uit: Beginstoffen → Reactieproducten
Als we het LEGO-voorbeeld gebruiken, krijg je: Bouwwerkje → drie verschillende LEGO-steentjes
Bij moleculen betekent dit dat je vóór de pijl één molecuul hebt dat na de pijl in meerdere elementen of atomen is veranderd. Bij ontleden is er dus altijd één beginstof voor de pijl en ontstaan er meerdere stoffen uit.
Fases van stoffen
Stoffen kunnen in verschillende fasen voorkomen. Dit is belangrijk om te vermelden in je reactieschema. Je doet dit door de fase achter de stof te zetten, tussen haakjes:
•Vaste stof: (s) van het Engelse 'solid'
•Vloeibaar: (l) van het Engelse 'liquid'
•Gas: (g) van het Engelse 'gas'
Voorbeeld: water is vloeibaar, dus dat schrijf je als water (l).
Ontleden van organische stoffen
Veel stoffen die we dagelijks tegenkomen, zijn organische stoffen. Denk aan papier, hout, brood, een appel en eigenlijk alles wat in de natuur voorkomt of van biologische oorsprong is. Een metaal is geen organische stof.
Als een organische stof ontleedt, ontstaan er altijd dezelfde reactieproducten. Een organische stof (s) ontleedt tot: Koolstof (s) + water (l) + witte rook (g)

Verbranden
Verbranden is ook een chemische reactie en lijkt een beetje op ontleden, maar er is een belangrijk verschil: bij verbranden is er altijd zuurstof (O₂) betrokken. Zuurstof is dus altijd één van de beginstoffen.
Een reactieschema maken voor verbranden
Het reactieschema bij verbranden ziet er zo uit: Brandstof + zuurstof → Verbrandingsproducten
De brandstof kan een vaste stof, vloeistof of gas zijn. Als je in een reactieschema zuurstof (O₂) voor de pijl ziet staan, weet je eigenlijk al meteen dat het om een verbranding gaat. De verbrandingsproducten zijn vaak koolstofdioxide (CO₂), water (H₂O) of allebei.
Hoe herken je een reactie?
Hoe weet je nou of er een chemische reactie heeft plaatsgevonden? Dat kun je zien, ruiken of voelen aan de hand van zeven reactieverschijnselen. Dit zijn veranderingen die je waarneemt met je eigen zintuigen:
1.Verandering van kleur: denk aan het zwart worden van eten als dit verbrandt.
2.Verandering van geur: je ruikt vaak goed als iets verbrand is.
3.Verandering van smaak: aangebrand eten smaakt niet meer lekker. Let op: niet alles is veilig om te proeven!
4.Warmte komt vrij: een verbranding kan warm aanvoelen.
5.Rook komt vrij: er ontstaat rook.
6.Vlammen komen vrij: je ziet vlammen.
7.Licht komt vrij: de reactie geeft licht af.
Wat gebeurt er als je een tosti aanbrandt?
Je kent het vast wel: de tosti is te lang in het tosti-ijzer blijven liggen en is helemaal zwart en vies geworden. Toch is er geen vuur bij de tosti gekomen. Hoe kan het dan dat hij is aangebrand? Een aangebrande tosti is geen verbranding, omdat er geen vuur of vlammen bij zijn geweest. Het is een ontleding.
Door de warmte in het tosti-ijzer gaan de moleculen van het brood ontleden. Brood is een organische stof. Zoals we eerder hebben gezien, komt bij de ontleding van een organische stof koolstof vrij als reactieproduct. Reactieschema voor de tosti: Organische stof (brood) (s) → Koolstof (s) + water (l) + witte rook (g)
De koolstof is een zwarte vaste stof en zorgt voor de zwarte kleur van je tosti. De smaak verandert en er kan wat rook (witte rook) vanaf komen. Dit zijn de reactieverschijnselen die je waarneemt. Het is dus een chemische reactie: de moleculen van het brood zijn veranderd in nieuwe stoffen die niet meer terug kunnen veranderen in brood.













