Hoe noem je de horizontale rijen en de verticale kolommen in het periodiek systeem?
Leerdoelen
•Je kunt van een element opzoeken in welke groep en periode het staat.
•Je kunt de atomen in het periodiek systeem onderverdelen in metalen en niet-metalen.
•Je kunt edelgassen en halogenen opzoeken.
•Je kunt de molecuulformules benoemen van zeven elementen die als twee-atomig molecuul voorkomen.
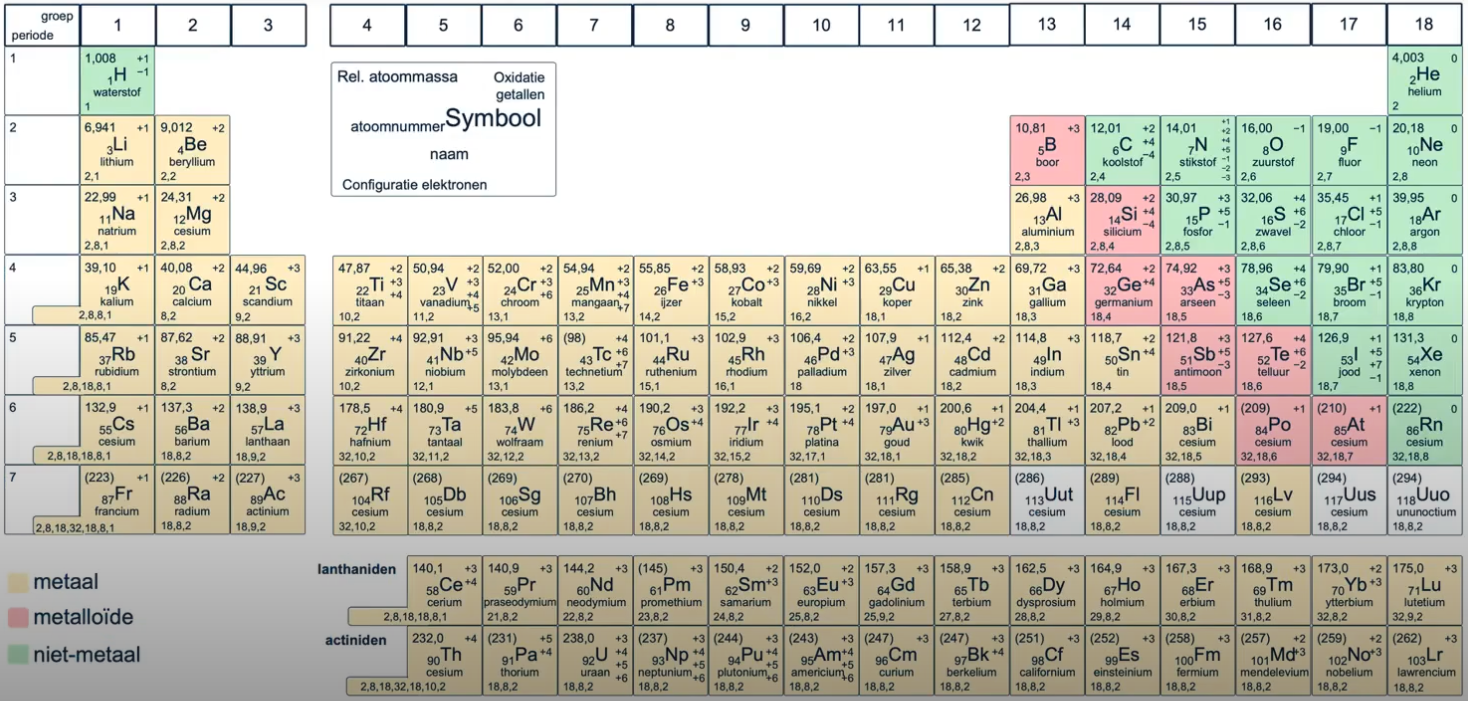
De basis van een element in het periodiek systeem
Elk vakje in het periodiek systeem representeert één uniek element.
In dit vakje vind je verschillende stukjes informatie:
•Symbool: dit zijn de letters die het element afkorten. De eerste letter is altijd een hoofdletter, en als er een tweede letter is, schrijf je die als een kleine letter (bijvoorbeeld Be voor beryllium, O voor zuurstof).
•Atoomnummer: dit getal staat meestal linksbovenin en geeft het aantal protonen in de kern van een atoom aan. Dit nummer bepaalt de identiteit van het element.
•Atoommassa: dit getal staat meestal rechtsbovenin en geeft de gemiddelde massa van de atomen van dat element weer, uitgedrukt in de eenheid u (unified atomic mass unit).
•Naam: de volledige naam van het element staat vaak onder het symbool (bijvoorbeeld beryllium).
Voorbeeld: Voor beryllium is het symbool Be, het atoomnummer is 4, de atoommassa is 9 u en de naam is beryllium.

Hoe is het periodiek systeem georganiseerd?
Een periode is een horizontale rij in het periodiek systeem. Alle elementen die naast elkaar staan, behoren tot dezelfde periode.
Een groep is een verticale kolom in het periodiek systeem. Elementen die onder elkaar staan, bevinden zich in dezelfde groep. Het bijzondere van elementen in dezelfde groep is dat ze vaak vergelijkbare chemische eigenschappen hebben.
Metalen en niet-metalen
Een derde indeling is gebaseerd op de aard van het element: is het een metaal of een niet-metaal? In de meeste periodieke systemen (zoals in de Binas) wordt dit aangegeven met kleuren. Er is een legenda die aangeeft welke kleur bij metalen en welke bij niet-metalen hoort. Soms zijn er ook metalloïden (stoffen met eigenschappen tussen metalen en niet-metalen in), maar deze worden in de Binas vaak onder de metalen geschaard.
Metalen en niet-metalen hebben heel verschillende stofeigenschappen:
•Glans: metalen zijn vaak glimmend (als ze gepolijst zijn), terwijl niet-metalen dof zijn.
•Buigzaamheid/Breekbaarheid: metalen zijn buigzaam; je kunt ze vaak vervormen zonder dat ze breken. Niet-metalen zijn daarentegen vaak breekbaar.
•Geleidbaarheid: metalen zijn goede geleiders van warmte en elektriciteit. Denk maar aan elektrische draden die van metaal zijn gemaakt. Niet-metalen zijn over het algemeen slechte geleiders van warmte en elektriciteit.
Bijzondere groepen: edelgassen en halogenen
Twee groepen in het periodiek systeem zijn extra bijzonder vanwege hun unieke eigenschappen:
Groep 18: edelgassen
•Groep 18 bevat de edelgassen. Dit zijn elementen die bijna niet reageren met andere stoffen. Ze zijn 'edel' omdat ze al een stabiele elektronenconfiguratie hebben en geen elektronen willen opnemen of afstaan.
Groep 17: halogenen
•Groep 17 bestaat uit de halogenen. Dit zijn niet-metalen die juist heel reactief zijn en gemakkelijk verbindingen aangaan, vooral met metalen. Wanneer een halogeen reageert met een metaal, ontstaat er vaak een zout (een niet-metaal plus een metaal).
Elementen die als twee-atomig molecuul voorkomen
Sommige elementen komen in de natuur niet voor als losse atomen, maar altijd in een verbinding. Als ze geen verbinding met een andere stof aangaan, vormen ze een molecuul met zichzelf, meestal als een twee-atomig (di-atomisch) molecuul. Dit betekent dat ze altijd als twee atomen aan elkaar vastzitten.
Deze zeven elementen moet je goed onthouden:
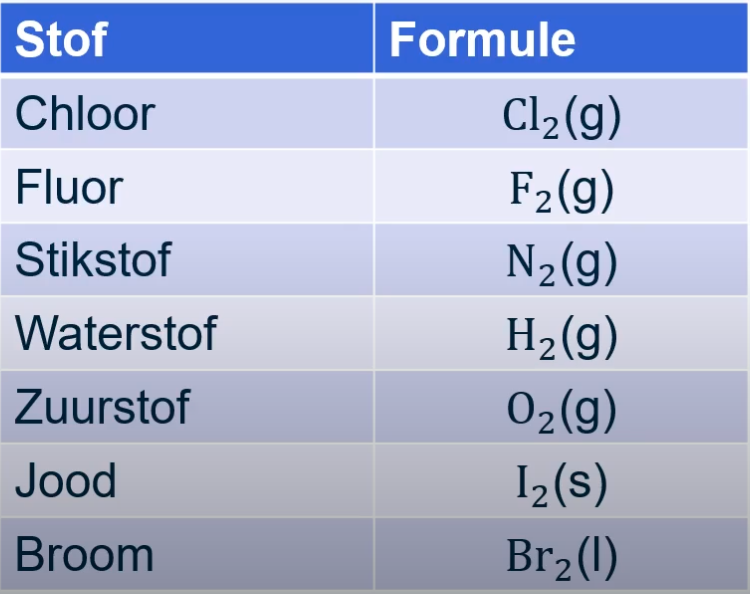
Er zijn handige ezelsbruggetjes om deze elementen te onthouden:
"Claire fietst naar haar oma in Breda":
Claire (Chloor)
Fietst (Fluor)
Naar (Stikstof)
Haar (Waterstof)
Oma (Zuurstof)
In (Jood)
Breda (Broom)
Een ander ezelsbruggetje is "BrINkLaHOF", waarbij de hoofdletters staan voor:
Br (broom), I (jood), N (stikstof), Cl (chloor), H (waterstof), O (zuurstof) en F (fluor).
Het is belangrijk om te weten dat als je een reactieformule opstelt, je bijvoorbeeld altijd moet opschrijven en niet alleen H, als waterstof als losse stof voorkomt. Een losse O (zuurstofatoom) of Cl (chlooratoom) bestaat niet zonder verbinding; ze zijn altijd met z'n tweeën () of vast aan een ander atoom in een molecuul (zoals in ).













