Zet de fases van een stof in de juiste volgorde, beginnend bij de fase waarin de moleculen het minst bewegen en eindigend bij de fase waarin ze het meest bewegen.
Leerdoelen
•Je kunt uitleggen wat moleculen zijn.
•Je kunt de drie fases benoemen waarin stoffen voorkomen: vast, vloeibaar en gas.
•Je kunt uitleggen wat er gebeurt wanneer stoffen uitzetten en krimpen.
•Je kunt de faseovergangen benoemen.
Wat zijn moleculen?
Als je heel erg inzoomt op bijvoorbeeld een glas water of zelfs op je eigen hand, zie je dat alles bestaat uit ontzettend kleine deeltjes. Deze deeltjes noemen we moleculen. Moleculen zijn de bouwstenen van alle stoffen om ons heen. Een watermolecuul is bijvoorbeeld specifiek voor water, en zo heeft elke stof zijn eigen soort moleculen.
Wat bijzonder is aan moleculen, is dat ze eigenlijk altijd bewegen. Zelfs in een vast voorwerp zoals een stoel trillen de moleculen op hun plek. Hoe en hoe snel moleculen bewegen, en hoeveel ruimte ze innemen, bepaalt de fase van een stof. Moleculen bestaan zelf ook weer uit nog kleinere deeltjes, namelijk atomen. Hierover leer je meer in een andere les.
De drie fases van stof
Stoffen kunnen in drie verschillende fases voorkomen: vast, vloeibaar en gas. Deze fases verschillen in de manier waarop de moleculen bewegen en geordend zijn.
Vaste fase
In de vaste fase zitten de moleculen allemaal op hun vaste plek. Ze bewegen wel, maar ze trillen alleen een klein beetje heen en weer. Je weet precies waar ze zijn. Denk bijvoorbeeld aan een ijsblokje: de watermoleculen zitten stevig aan elkaar en vormen een vaste vorm.
Vloeibare fase
In de vloeibare fase bewegen de moleculen iets meer dan in de vaste fase. Ze glijden langs elkaar heen en hebben iets meer ruimte nodig. Hierdoor heeft een vloeistof geen vaste vorm, maar neemt het de vorm aan van het vat waarin het zit. Water in een glas is hier een goed voorbeeld van. De moleculen zijn nog steeds dicht bij elkaar, maar ze kunnen wel van plek wisselen.
Gasvormige fase
In de gasvormige fase bewegen de moleculen heel veel en helemaal vrij. Ze zitten heel ver uit elkaar en verspreiden zich door de hele beschikbare ruimte. Ze hebben de meeste ruimte nodig. Denk aan waterdamp; de moleculen vliegen overal door de lucht. Een gas heeft geen vaste vorm en geen vast volume.
Een schoolfeest als voorbeeld
Om het verschil tussen de fases beter te begrijpen, kun je denken aan leerlingen op een schoolfeest:
•Vaste fase: Dit zijn de leerlingen die aan de rand van de zaal staan. Ze bewegen een beetje, misschien met hun hoofd of een voet, maar blijven vooral op hun vaste plek bij dezelfde vrienden.
•Vloeibare fase: Dit zijn de meeste leerlingen die gewoon een beetje op de dansvloer staan te dansen. Ze bewegen iets meer en hebben wat meer ruimte nodig, maar blijven wel bij hun vrienden in de buurt.
•Gasvormige fase: Dit zijn de leerlingen die het heel erg naar hun zin hebben en overal dansen. Je bent ze de hele avond kwijt! Ze hebben heel veel ruimte nodig en bewegen heel wild door de hele zaal.
Uitzetten en krimpen
Hoe snel moleculen bewegen, hangt af van de temperatuur. Als de temperatuur van een stof stijgt, krijgen de moleculen meer energie en gaan ze meer bewegen. Wanneer moleculen meer bewegen, hebben ze ook meer ruimte nodig. Hierdoor zal het materiaal uitzetten. Dit betekent dat het groter wordt. Denk maar aan een thermometer; de vloeistof in de thermometer zet uit als het warmer wordt.
Het tegenovergestelde van uitzetten is krimpen. Als de temperatuur omlaag gaat, hebben de moleculen minder energie. Met minder energie willen ze minder bewegen en hebben ze ook minder ruimte nodig. Hierdoor zal het materiaal krimpen en kleiner worden.
Faseovergangen
Als de temperatuurverandering extreem genoeg is, kunnen stoffen van de ene fase naar de andere overgaan. Dit noemen we een faseovergang. Er zijn zes verschillende faseovergangen.
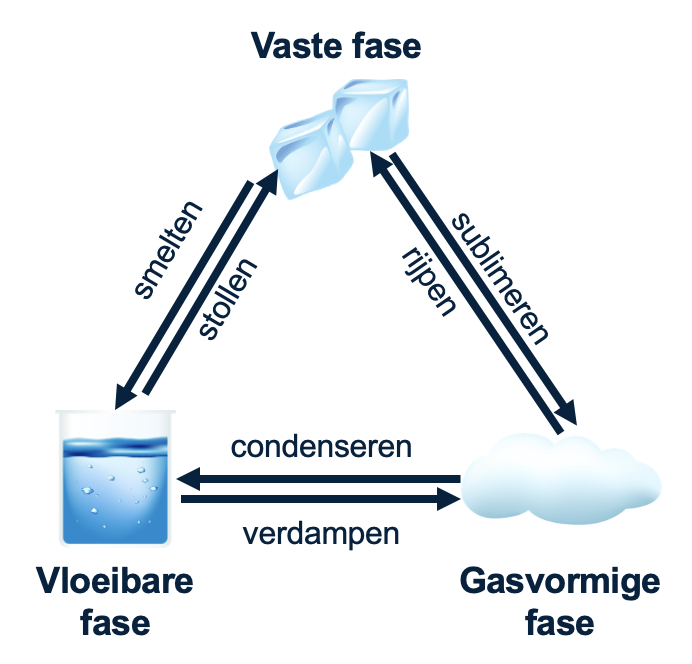
Van vast naar vloeibaar en terug
•Smelten: Als een vaste stof warm wordt en genoeg energie krijgt, gaan de moleculen zo hard bewegen dat ze hun vaste plek verlaten en langs elkaar heen gaan glijden. De stof wordt dan vloeibaar. Denk aan ijs dat smelt en water wordt.
•Stollen (of bevriezen): Het tegenovergestelde gebeurt als een vloeistof heel erg koud wordt en energie verliest. De moleculen gaan minder bewegen en nemen weer vaste posities in. De vloeistof wordt dan vast. Wanneer water ijs wordt, spreken we vaak van bevriezen. In de natuurkunde noemen we dit stollen, omdat dit voor alle stoffen geldt.
Van vloeibaar naar gas en terug
•Verdampen: Als een vloeistof warm wordt en veel energie krijgt, gaan de moleculen zo hard en vrij bewegen dat ze loskomen van elkaar en een gas worden. Dit zie je gebeuren als water in een waterkoker gaat koken en waterdamp wordt.
•Condenseren: Als een gas afkoelt en energie verliest, gaan de moleculen minder hard en vrij bewegen. Ze komen dichter bij elkaar en worden weer een vloeistof. Dit zie je 's ochtends op het gras: waterdamp in de lucht koelt af en vormt kleine waterdruppeltjes op het gras, ook wel dauw genoemd.
Van vast naar gas en terug
Deze faseovergangen zie je minder vaak in het dagelijks leven, omdat ze alleen onder specifieke omstandigheden plaatsvinden.
•Sublimeren: Dit is de overgang van een vaste stof direct naar een gas, zonder eerst vloeibaar te worden. Droogijs (vaste koolstofdioxide) is hier een bekend voorbeeld van; het lijkt te roken zonder te smelten.
•Rijpen: Dit is de overgang van een gas direct naar een vaste stof, zonder eerst vloeibaar te worden. Wanneer het heel koud is, kan waterdamp uit de lucht direct overgaan in ijskristallen, zoals rijp op takken.
Waarom kan een fietsband ontploffen in de zon?
Een fietsband, vaak zwart van kleur, neemt veel energie op van de zon. Hierdoor stijgt de temperatuur binnenin de band aanzienlijk.
1.De lucht in de fietsband wordt warmer.
2.De gasvormige moleculen in de lucht krijgen meer energie.
3.Met meer energie gaan de moleculen sneller en wilder bewegen.
4.Doordat de moleculen meer bewegen en meer ruimte nodig hebben, zet de lucht in de band uit.
5.Als de lucht in de band zoveel uitzet dat de band de druk niet meer kan houden, zal de band scheuren of zelfs ontploffen.
Hoewel dit vaak extreme temperaturen vereist, is het altijd goed om voorzichtig te zijn. Parkeer je fiets of auto op een warme dag liever in de schaduw om problemen te voorkomen!













