Welke eigenschap van een element kun je gebruiken om te bepalen of het een metaal is of een niet-metaal?
Leerdoelen
•Je kunt uitleggen wat moleculen zijn.
•Je kunt voorbeelden noemen van verschillende atomen.
•Je kunt elementen indelen in metalen en niet-metalen.
•Je kunt onderscheiden wanneer een stof een metaal, een zout of een moleculaire stof is.
Atomen en moleculen
Alles om je heen is opgebouwd uit kleine deeltjes. Als je heel ver inzoomt, zie je dat alles bestaat uit moleculen. Maar je kunt nog verder inzoomen! Dan ontdek je dat die moleculen zelf weer bestaan uit nog kleinere deeltjes: de atomen. Denk aan atomen als de bouwstenen van alles.
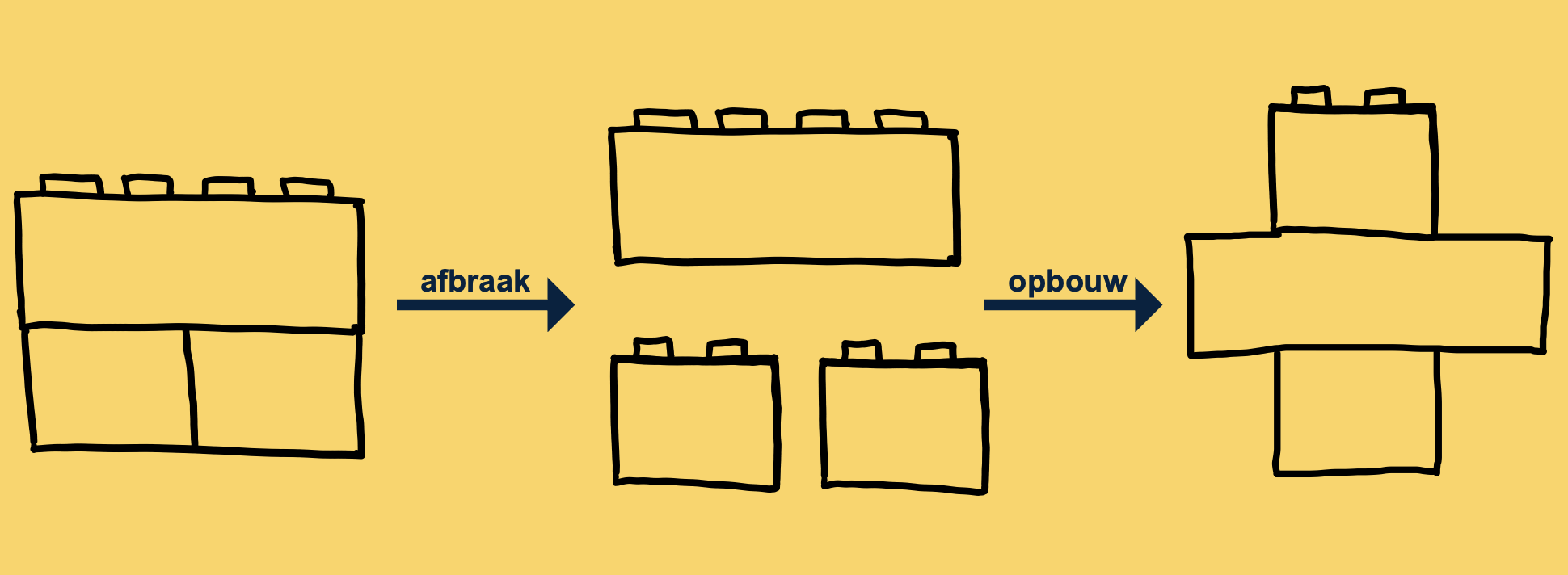
Stel je voor: een atoom is één bouwsteen. Als je verschillende bouwstenen aan elkaar klikt, krijg je een klein bouwwerkje, en dat noemen we een molecuul. Als je heel veel van zulke bouwwerkjes (moleculen) bij elkaar doet, krijg je een groter ‘gebouw’, oftewel de stof die je in het dagelijks leven ziet.
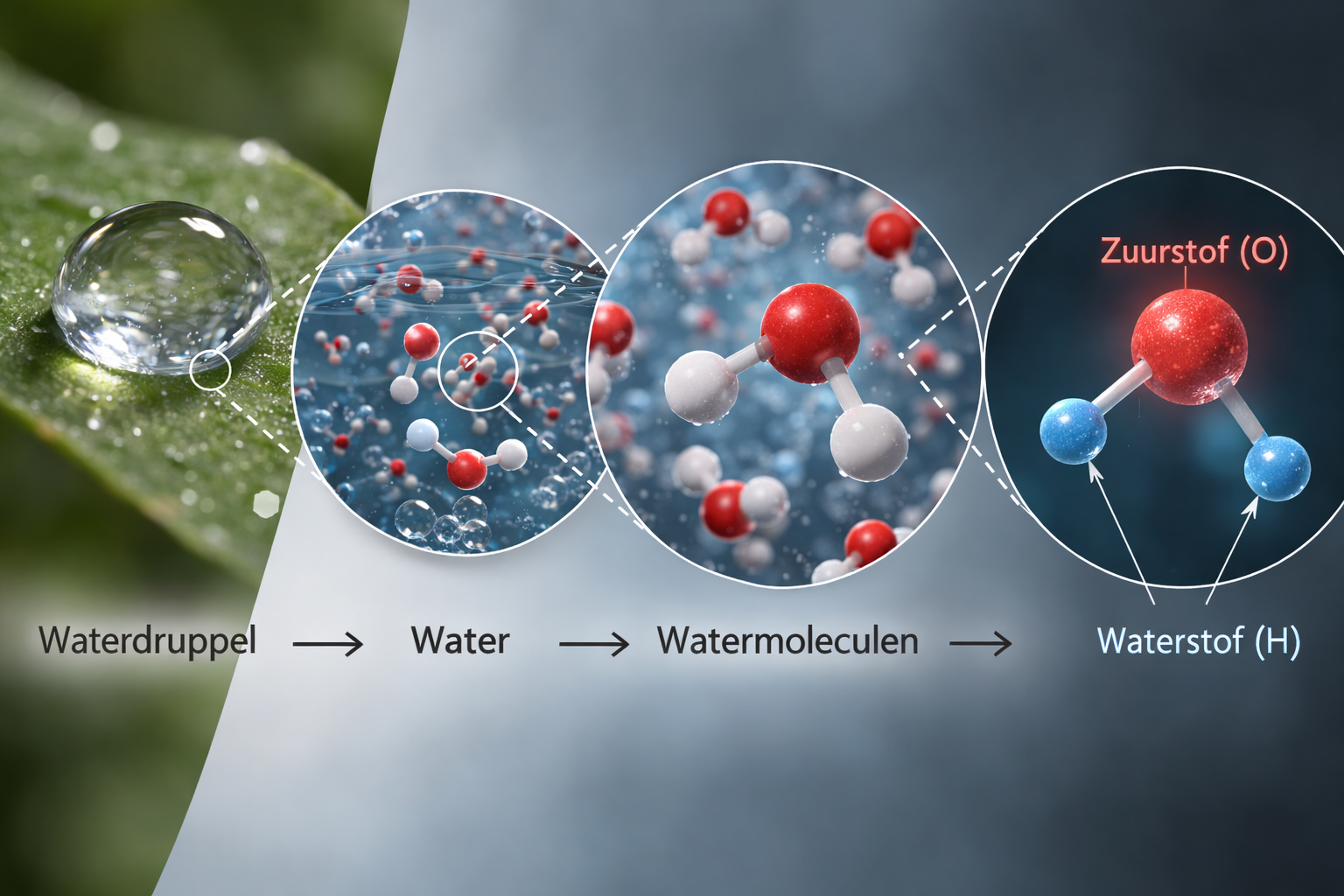
Neem bijvoorbeeld water. Water is een stof. Als je inzoomt op water, zie je een watermolecuul. Als je nog verder inzoomt, zie je dat zo’n watermolecuul bestaat uit twee soorten atomen: twee waterstofatomen (H) en één zuurstofatoom (O). De formule van water is dan ook H₂O. Deze kleine atomen kunnen niet meer kleiner gemaakt worden zonder ze kapot te maken. Het woord atoom komt zelfs van het Griekse 'a-tomos', wat 'niet deelbaar' betekent. Deze atomen noemen we ook wel elementen. Atomen en elementen zijn dus hetzelfde.
Om het makkelijker te maken, geven we atomen of elementen ook symbolen of afkortingen. Zo wordt kalium afgekort met de letter K, koolstof met C, waterstof met H en zuurstof met O.
De verschillende soorten atomen
Er zijn ongeveer honderd verschillende soorten atomen, dus honderd verschillende soorten bouwstenen. Deze atomen of elementen kun je onderverdelen in twee groepen: metalen en niet-metalen. Het verschil is vrij simpel: door een metaal kan elektriciteit heen, door een niet-metaal kan dat niet. Als je dus wilt weten of een element een metaal is, kun je jezelf afvragen: kan hier elektriciteit doorheen?
Het is belangrijk dat je een aantal van de meest voorkomende elementen en hun symbolen kent, zoals koolstof (C), waterstof (H) en zuurstof (O). Je hoeft vaak niet alle honderd elementen uit je hoofd te leren, maar dit is afhankelijk van je docent. Veel belangrijker is dat je weet waar je ze kunt opzoeken, bijvoorbeeld in een tabel in je NaSk-boek. Zo'n tabel vertelt je dan ook of een element een metaal of een niet-metaal is. Zuurstof is bijvoorbeeld een niet-metaal, terwijl kalium, koper en aluminium metalen zijn.
Naam element | Symbool | Soort element |
|---|---|---|
Zuurstof | O | niet-metaal |
Kalium | K | metaal |
Koper | Cu | metaal |
Aluminium | Al | metaal |
Waterstof | H | niet-metaal |
Koolstof | C | niet-metaal |
Hoe atomen stoffen vormen
Nu je weet dat er metalen en niet-metalen elementen bestaan, kunnen we kijken wat er gebeurt als we deze bouwstenen met elkaar combineren. Door atomen aan elkaar te plakken, oftewel te verbinden, maken we een stof of een molecuul. Er zijn drie hoofdsoorten stoffen die je kunt maken door atomen te verbinden:
1.Metalen stoffen: Deze ontstaan wanneer je twee of meer metaalelementen aan elkaar plakt. Denk aan het combineren van koper en aluminium. Het resultaat is dan een metaalstof (of een legering, wat een mengsel is van metalen).
2.Zouten: Een zout ontstaat als je een metaalelement en een niet-metaalelement aan elkaar plakt. Een voorbeeld is natrium (een metaal) plus chloor (een niet-metaal). Dit levert een zout op, namelijk natriumchloride (keukenzout).
3.Moleculaire stoffen: Deze stoffen worden gevormd wanneer twee of meer niet-metaalelementen met elkaar verbinden. Water is hier een perfect voorbeeld van. Het bestaat uit waterstof (een niet-metaal) en zuurstof (ook een niet-metaal). Plak je deze twee niet-metalen aan elkaar, dan krijg je een moleculaire stof.
Wat is een chemische reactie?
Bij een chemische reactie verandert het bouwwerkje, dus het molecuul, wel. Moleculen kunnen uit elkaar vallen en opnieuw rangschikken om nieuwe moleculen te vormen. De atomen zelf veranderen echter niet. Denk eraan als het uit elkaar halen van een LEGO-bouwwerkje in losse steentjes en er vervolgens een nieuw bouwwerkje van maken met exact dezelfde steentjes. De steentjes (atomen) zijn nog steeds dezelfde steentjes als voor de reactie, maar het bouwwerkje (het molecuul) is anders.
Dus bij een chemische reactie:
•De moleculen veranderen.
•De atomen veranderen niet.