Vul deze aan.
Leerdoelen
•Je kunt uitleggen wat een samengesteld ion is.
•Je kunt verschillende samengestelde ionen benoemen.
•Je kunt verhoudingsformules voor samengestelde ionen maken.
Wat is een samengesteld ion?
Een samengesteld ion is een molecuul dat een elektrische lading heeft. In tegenstelling tot gewone ionen, die uit één atoom bestaan, bestaat een samengesteld ion uit meerdere atomen van verschillende elementen die samen één geladen deeltje vormen. Omdat het deeltje een lading heeft, noemen we het een ion. Het heet samengesteld omdat het uit meerdere atoomsoorten bestaat.
Twee varianten samengestelde ionen
Positieve samengestelde ionen
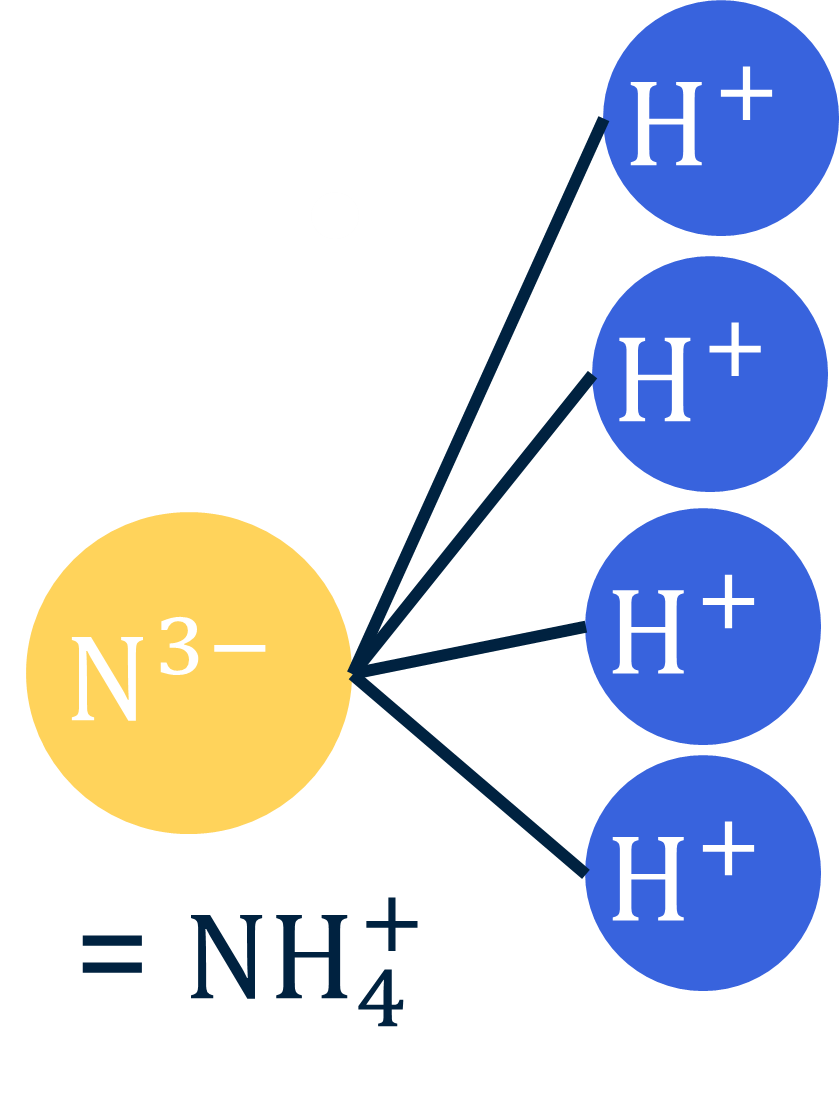
Deze ontstaan wanneer er meer plusjes dan minnetjes zijn. Stel je voor: je hebt een stikstof-ion met drie minnetjes (N³⁻) en je plakt daar vier waterstofionen met één plusje (H⁺) aan vast. Je hebt dan 3 minnetjes van de N en 4 plusjes van de H. Samen heb je 4 plusjes en 3 minnetjes, dus blijft er één plusje over. Het samengestelde ion dat hieruit ontstaat, is NH₄⁺. De index 4 geeft aan dat er vier waterstofatomen zijn en het plusje de totale lading van het ion.
Voorbeeld: ammonium-ion (NH₄⁺)
Stikstof-ion: N³⁻ → 3 minladingen
Waterstofionen: 4 × H⁺ → 4 plusladingen
Berekening van de lading: 4⁺ + 3⁻ = 1⁺ over
Resultaat: NH₄⁺ (ammonium-ion)
Negatieve samengestelde ionen
Deze ontstaan wanneer er meer minnetjes dan plusjes zijn. Stel je voor: je hebt een zuurstof-ion met twee minnetjes (O²⁻) en je plakt daar één waterstofion met één plusje (H⁺) aan vast. Je hebt dan 2 minnetjes van de O en 1 plusje van de H. Samen heb je 1 plusje en 2 minnetjes, dus blijft er één minnetje over. Het samengestelde ion dat hieruit ontstaat, is OH⁻.
Voorbeeld: hydroxide-ion (OH⁻)
Zuurstof-ion: O²⁻ → 2 minladingen
Waterstofion: H⁺ → 1 pluslading
Berekening van de lading: 1⁺ + 2⁻ = 1⁻ over
Resultaat: OH⁻ (hydroxide-ion)
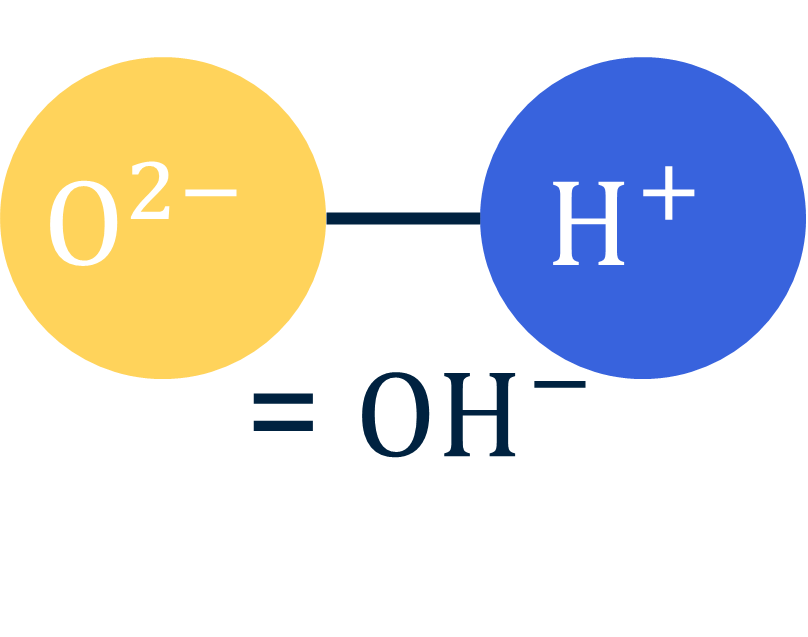
Belangrijke samengestelde ionen
Een aantal samengestelde ionen moet je gewoon kennen en uit je hoofd leren. Dit is belangrijk omdat je ze nodig hebt om zouten te maken. Het is vooral cruciaal dat je het juiste aantal plusjes of minnetjes van elk ion onthoudt. Let goed op welke tabel met samengestelde ionen je precies moet leren, want dit kan verschillen per docent voor een schoolexamen, of voor het eindexamen.
Formule | Naam |
|---|---|
OH- | hydroxide-ion |
NO3- | nitraation |
CO32- | carbonaat-ion |
SO42- | sulfaation |
PO43- | fosfaation |
NH4+ | ammonium-ion |
Verhoudingsformules maken met samengestelde ionen
Het maken van een verhoudingsformule voor samengestelde ionen werkt hetzelfde als voor enkelvoudige ionen. Het belangrijkste principe is dat een zout altijd neutraal is; het bevat dus evenveel positieve als negatieve ladingen.
Volg deze stappen om een verhoudingsformule te maken:
Stap 1: Naam van het zout opschrijven
Begin met het opschrijven van de naam van het zout. Wij gebruiken lood(IV)sulfaat. De (IV) achter lood betekent dat lood in dit geval een lading heeft van 4+. (IV) is Latijn voor vier. Het sulfaation vind je in de Binas of moet je uit je hoofd kennen.
Stap 2: Symbolen opschrijven
Schrijf de symbolen van de ionen op. Let op: je schrijft altijd eerst het positieve ion op. Voor lood(IV) is dit Pb⁴⁺. Voor sulfaat is dit SO₄²⁻.
Stap 3: Zorgen voor evenveel plusjes en minnetjes
Nu moet je ervoor zorgen dat de totale positieve lading gelijk is aan de totale negatieve lading. Dit kun je doen met een tabel.
Om de ladingen gelijk te maken, moeten we twee keer zoveel sulfaationen hebben (2 x 2 minnetjes = 4 minnetjes). Dus, je hebt 1 loodion nodig en 2 sulfaationen.
Ion | Lading | Aantal nodig | Totale lading |
|---|---|---|---|
Pb⁴⁺ | +4 | 1 | +4 |
SO₄²⁻ | -2 | 2 | -4 |
Stap 4: Verhoudingsformule netjes opschrijven
We hebben 1 loodion (Pb) en 2 sulfaationen (SO₄). Als er maar één ion is, zoals lood (Pb), hoef je geen index te noteren. Voor het sulfaation (SO₄) hebben we er twee nodig, dus komt er een index 2 bij. Het grote verschil met enkelvoudige ionen is dat je het hele samengestelde ion (SO₄) tussen haakjes zet voordat je de index eraan plakt. Dit doe je alleen als de index groter is dan 1. De verhoudingsformule wordt dan: Pb(SO₄)₂.














