Wat betekenen de woorden 'mono' en 'poly'?
Leerdoelen
•Je kunt uitleggen wat polymerisatie is.
•Je kunt de reactie van polymerisatie correct tekenen.
•Je kunt minimaal twee verschillende soorten plastic benoemen en de belangrijkste eigenschappen ervan beschrijven.
Monomeren en polymeren
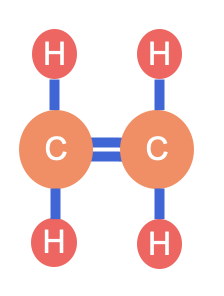
Kunststof bestaat uit hele kleine bouwsteentjes die we monomeren noemen. Het woord mono betekent 'één', een monomeer is één molecuul. Een bekend voorbeeld is etheen. Dit is een alkeen, wat betekent dat het twee koolstofatomen (C) heeft die met een dubbele binding aan elkaar vastzitten, met daaraan ook vier waterstofatomen (H).
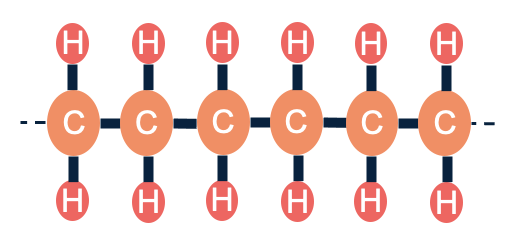
Als je heel veel van zulke monomeren aan elkaar plakt, ontstaat er een lange keten. Deze lange keten noemen we een polymeer. Het woord poly betekent 'veel'. Dus een polymeer is een groot molecuul dat bestaat uit veel herhalende monomeren. Als je bijvoorbeeld veel etheenmoleculen aan elkaar plakt, krijg je polyetheen.
Omdat er veel verschillende soorten monomeren bestaan, zijn er ook veel verschillende kunststoffen, elk met unieke eigenschappen.
Polymerisatie
Het proces waarbij monomeren aan elkaar koppelen tot een polymeer heet polymerisatie. Dit gebeurt niet zomaar; er is een speciaal stappenplan voor. Let op: dit werkt alleen als het monomeer een dubbele binding heeft, zoals etheen of tetrafluoretheen. De dubbele binding is nodig om de ketenreactie te starten.
Het stappenplan voor het tekenen van een polymeer
Laten we de polymerisatie van tetrafluoretheenals voorbeeld nemen. Tetra betekent vier; het monomeer heeft vier fluoratomen (F) en twee koolstofatomen (C).
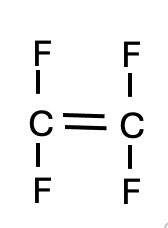
Stap 1: Teken de structuurformule van het monomeer. Een koolstofatoom (C) wil altijd vier bindingen hebben. In tetrafluoretheen zijn er twee C-atomen, elk verbonden met twee F-atomen. Om aan vier bindingen te komen, zit er een dubbele binding tussen de twee C-atomen.
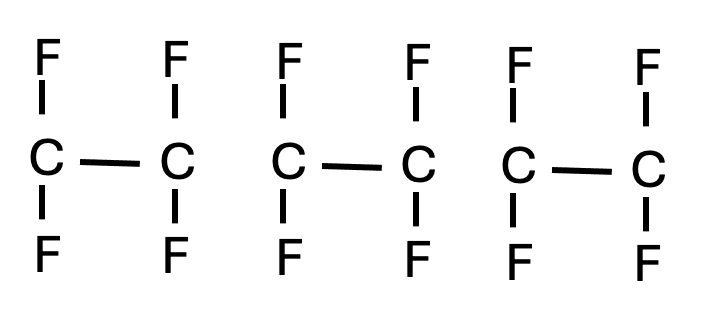
Stap 2: Teken meerdere monomeren naast elkaar, zonder de dubbele binding. Bij polymerisatie opent de dubbele binding zich, zodat de monomeren aan elkaar kunnen koppelen. Teken minstens drie monomeren naast elkaar, maar laat de dubbele binding weg en verbind ze nog niet met elkaar.
Stap 3: Verbind de monomeren en geef de lange keten weer. Nu kun je de opengeklapte bindingen van de monomeren met elkaar verbinden. Om te laten zien dat de keten aan beide kanten nog veel langer kan zijn, zet je stippellijntjes aan de uiterste koolstofatomen. Dit geeft aan dat er nog meer monomeren aan vast kunnen zitten.
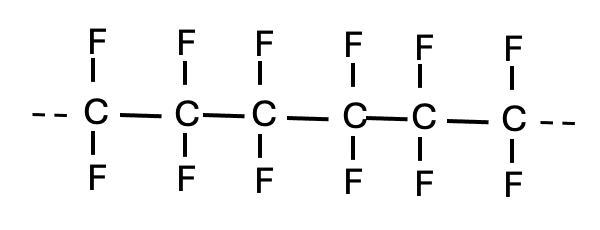
Formule van een polymeer
Je kunt een polymeer ook met een formule weergeven. Je schrijft de formule van het monomeer tussen haakjes, met een kleine n rechtsonder de haakjes. De n staat voor 'heel veel' van dit monomeer. Voor poly(tetrafluoretheen) schrijf je bijvoorbeeld.
Thermoplasten en thermoharders
Niet alle kunststoffen zijn hetzelfde. Ze verschillen in eigenschappen en hoe ze reageren op bijvoorbeeld hitte. Er zijn twee belangrijke soorten plastic die je moet kennen: thermoplasten en thermoharders.
Thermoplasten
Bij thermoplasten liggen de polymeerketens los van elkaar. Ze zijn niet met elkaar verbonden, net zoals losse oplaadkabels netjes naast elkaar liggen.
Door deze losse structuur zijn thermoplasten:
•Gemakkelijk vervormbaar: Je kunt ze buigen en bewegen.
•Smeltbaar: Bij verhitting smelten ze. Dit betekent dat je ze in een andere vorm kunt gieten om er iets nieuws van te maken.
•Recyclebaar: Omdat ze smelten, kunnen ze opnieuw worden verwerkt. Denk bijvoorbeeld aan een plastic waterflesje. Als je het leegdrinkt, kun je het recyclen. Dat waterflesje is dus een thermoplast.
Thermoharders
Bij thermoharders zijn de polymeerketens wel met elkaar verbonden. Ze zitten in elkaar verstrengeld, alsof al die oplaadkabels helemaal in de knoop zitten en aan elkaar zijn vastgemaakt.
Deze sterke verbindingen zorgen ervoor dat thermoharders:
•Erg sterk: Ze zijn moeilijk uit elkaar te krijgen of te buigen.
•Niet-smeltbaar: Als je een thermoharder verhit, zal hij niet smelten en van vorm veranderen. In plaats daarvan zal hij verbranden.
•Niet-recyclebaar: Omdat ze niet smelten, kunnen thermoharders niet eenvoudig worden omgesmolten en hergebruikt. Dit maakt ze slechter voor het milieu dan thermoplasten. Voorbeelden zijn onderdelen van panhandvatten of de behuizing van elektrische stekkers.














