Wat is de definitie van het kookpunt van een zuivere stof?
Leerdoelen
•Je kunt uitleggen wat er gebeurt met de temperatuur van een stof tijdens een faseovergang.
•Je kunt de begrippen kookpunt, smeltpunt, vriespunt en stolpunt benoemen en aanwijzen in een diagram.
•Je kunt het verschil in temperatuurverloop tussen een zuivere stof en een mengsel beschrijven.
•Je kunt uitleggen hoe je het kookpunt en stolpunt van water kunt veranderen door een stof toe te voegen.
Kookpunt en verdampen
Wanneer je water verhit, stijgt de temperatuur totdat het begint te koken. Het kookpunt is de temperatuur waarbij de hele vloeistof overgaat naar een gas. Deze faseovergang noemen we verdampen. Voor water ligt dit punt op honderd graden Celsius. Een interessante vraag is waarom water nooit warmer kan worden dan honderd graden Celsius. Dit komt doordat bij het kookpunt alle energie die je toevoegt, wordt gebruikt om de vloeistof te laten verdampen. Pas als alle vloeistof een gas is geworden, kan de temperatuur weer verder stijgen.
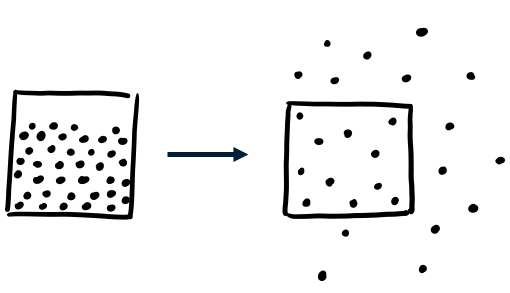
Smelten en het smeltpunt
Naast koken kennen we ook het proces waarbij een vaste stof een vloeistof wordt. Dit noemen we smelten. De temperatuur waarbij dit gebeurt, is het smeltpunt. Bij water is dit nul graden Celsius. De vaste vorm van water noemen we ijs. Op het moment dat ijs smelt, blijft de temperatuur precies nul graden totdat al het ijs is veranderd in vloeibaar water.
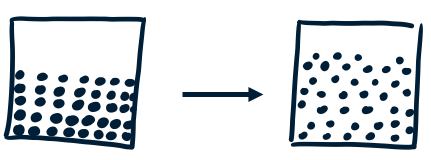
Stollen en bevriezen
Het omgekeerde van smelten is stollen. Dit is de faseovergang van een vloeistof naar een vaste stof. De temperatuur waarbij dit gebeurt, noemen we het stolpunt. Er is een speciale regel voor water: alleen bij water mag je stollen ook wel bevriezen noemen. Het punt waarop dit gebeurt, heet dan het vriespunt. Voor zuiver water is dit nul graden Celsius. Bij andere stoffen gebruik je dus altijd de term stollen.
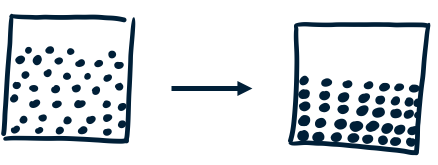
Diagrammen van een zuivere stof
In de natuurkunde kijken we vaak naar een zuivere stof. Dit is een stof die uit maar één soort molecuul bestaat. Als je van een zuivere stof een diagram maakt waarin je de temperatuur tegen de tijd uitzet, zie je tijdens de faseovergang een horizontale lijn. Deze horizontale lijn ontstaat omdat de temperatuur niet stijgt of daalt tijdens de faseovergang. Alle energie wordt namelijk gebruikt om de overgang van de ene fase naar de andere fase mogelijk te maken. Omdat elk kookpunt en smeltpunt uniek is voor een specifieke stof, noemen we dit een stofeigenschap. Hierdoor kun je een onbekende stof herkennen; als een vloeistof precies bij honderd graden Celsius kookt, weet je zeker dat het water is.
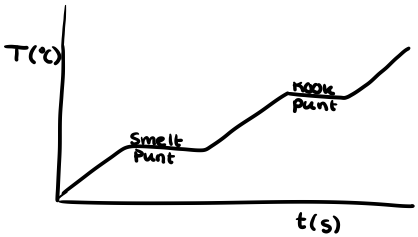
Mengsels en trajecten
Wanneer je een andere stof toevoegt aan een zuivere stof, krijg je een mengsel. Een mengsel bevat meerdere soorten moleculen. Hierdoor verandert het gedrag tijdens het koken of smelten. In een diagram van een mengsel zie je geen horizontale lijn, maar een schuine lijn of een bochtje. We spreken dan niet meer van een punt, maar van een traject.
Bij een mengsel heb je dus een kooktraject, een smelttraject of een stoltraject. Dit betekent dat de faseovergang plaatsvindt over een bepaald bereik van temperaturen en niet op één vast getal.
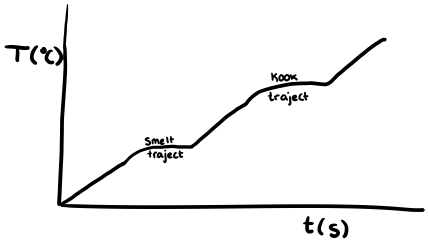
Kook- en smeltpunten beïnvloeden
Je kunt de eigenschappen van water veranderen door er een mengsel van te maken. Een bekend voorbeeld is het toevoegen van zout aan water. Zout zorgt ervoor dat het kook- en smeltpunt van water verandert.
koken: door zout toe te voegen verhoog je het kookpunt, waardoor het water warmer kan worden dan honderd graden Celsius voordat het kookt.
strooien: in de winter strooien we zout op de weg om gladheid te voorkomen. Het zoute water blijft dan langer vloeibaar en bevriest pas bij een temperatuur die lager is dan nul graden Celsius.













